
| A. | 升高温度,可以加快反应速率 | |
| B. | 降低温度,可以加快反应速率 | |
| C. | 在上述条件下,SO2能完全转化为SO3 | |
| D. | 任何情况,达到平衡时,SO2和SO3的浓度都一定相等 |
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 在稀溶液中:H++OH-═H2O;△H=-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量等于57.3kJ | |
| B. | 由4P(s,红磷)═P4(s,白磷):△H>0可知,白磷的热稳定性比红磷大 | |
| C. | 已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol-1,则H2的燃烧热等于241.8 kJ•mol-1 | |
| D. | 己知:S(g)+O2(g)═SO2(g);△H1及S(s)+O2(g)═SO2(g):△H2,则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 乙醇与钠反应:2CH3CH2O-+2H++2Na→2CH3CH2ONa+H2↑ | |
| C. | 苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 苯酚溶液中加入溴水: +3B2→ +3B2→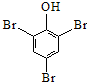 ↓+3H++3Br- ↓+3H++3Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③④⑤⑥ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 201.4 g | B. | 212.0 g | C. | 21.2 g | D. | 100.7 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,电子排布式1s22s22p63s23p63d14s2.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.
,电子排布式1s22s22p63s23p63d14s2.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.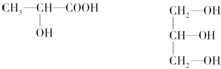
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com