

a×
| ||
| 10 |


科目:高中化学 来源: 题型:
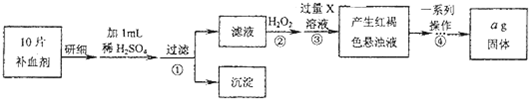
| A、氧气和臭氧的混合物1.6g中含有6.02×1022个氧原子 |
| B、2.8克氮气和一氧化碳混合气体的原子数目为0.2NA |
| C、1.12L氯气中含有6.02×1022个氯原子 |
| D、标准状况下,1.12L的H2O所含的原子数大于0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ①Li-甲胺 |
| ②H+H2O |
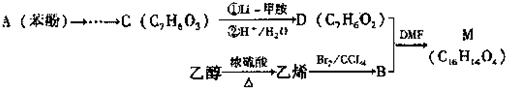
查看答案和解析>>
科目:高中化学 来源: 题型:
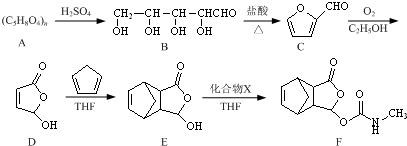
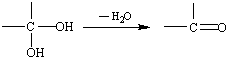
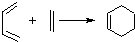
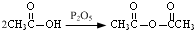
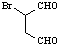 和
和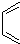 为原料合成
为原料合成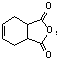 ,请设计合成路线(注明反应条件).
,请设计合成路线(注明反应条件).| 浓硫酸 |
| 170℃ |
| Br2 |

查看答案和解析>>
科目:高中化学 来源: 题型:

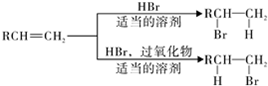
 )的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任用).合成路线流程图示例如下:| 浓硫酸 |
| 170℃ |
| Br2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com