
【题目】有丙炔和氢气的混合气体5L,在催化剂作用下,经充分反应后得到的气体的体积为V(所有体积均在同温同压下测定)。
(1)若将上述5L气体在氧气中完全燃烧生成二氧化碳和水,消耗同温同压下氧气的体积V(O2)为___(取值范围)。
(2)若氢气的体积为1L,反应后的体积V=___L。
(3)若氢气在混合气体中的体积分数为x,试用x表示反应后的体积V=___。
【答案】2.5L<V(O2)<20L 4 0<x≤![]() ,V=(5-5x)L;
,V=(5-5x)L;![]() <x<1,V=(10x-5)L
<x<1,V=(10x-5)L
【解析】
在催化剂作用下,丙炔和氢气发生的反应可能为①C3H4+H2![]() C3H6,②C3H4+2H2
C3H6,②C3H4+2H2![]() C3H8,当V(C3H4):V(H2)<
C3H8,当V(C3H4):V(H2)<![]() 时,氢气过量,剩余气体的气体体积为C3H8和剩余H2的混合物;当V(C3H4):V(H2)≥
时,氢气过量,剩余气体的气体体积为C3H8和剩余H2的混合物;当V(C3H4):V(H2)≥![]() 时,氢气不足,得到的产物是C3H6或C3H8或二者的混合物。
时,氢气不足,得到的产物是C3H6或C3H8或二者的混合物。
(1)若5L丙炔和氢气的混合气体全部为丙炔,丙炔完全燃烧的化学方程式为C3H4+4O2 ![]() 3CO2+2H2O,由化学方程式可知,5L丙炔完全燃烧消耗同温同压下氧气的体积V(O2)为5L×4=20L,若5L丙炔和氢气的混合气体全部为氢气,氢气完全燃烧的化学方程式为2H2+O2
3CO2+2H2O,由化学方程式可知,5L丙炔完全燃烧消耗同温同压下氧气的体积V(O2)为5L×4=20L,若5L丙炔和氢气的混合气体全部为氢气,氢气完全燃烧的化学方程式为2H2+O2 ![]() 2H2O,由化学方程式可知,5L氢气完全燃烧消耗同温同压下氧气的体积V(O2)为5L×
2H2O,由化学方程式可知,5L氢气完全燃烧消耗同温同压下氧气的体积V(O2)为5L×![]() =2.5L,则5L气体在氧气中完全燃烧消耗同温同压下氧气的体积V(O2)为2.5L<V(O2)<20L,故答案为:2.5L<V(O2)<20L;
=2.5L,则5L气体在氧气中完全燃烧消耗同温同压下氧气的体积V(O2)为2.5L<V(O2)<20L,故答案为:2.5L<V(O2)<20L;
(2)若氢气的体积为1L,丙炔的体积为4L,则在催化剂作用下,丙炔和氢气发生反应C3H4+H2![]() C3H6,由方程式可知氢气不足量,反应得到丙炔和丙烯的混合气体,由碳原子个数守恒可知,反应后丙炔和丙烯的混合气体体积与反应前丙炔气体体积相同,为4L,故答案为:4;
C3H6,由方程式可知氢气不足量,反应得到丙炔和丙烯的混合气体,由碳原子个数守恒可知,反应后丙炔和丙烯的混合气体体积与反应前丙炔气体体积相同,为4L,故答案为:4;
(3)在催化剂作用下,丙炔和氢气发生的反应可能为①C3H4+H2![]() C3H6,②C3H4+2H2
C3H6,②C3H4+2H2![]() C3H8,当V(C3H4):V(H2)<
C3H8,当V(C3H4):V(H2)<![]() 时,即
时,即![]() <x<1,氢气过量,剩余气体的气体体积为C3H8和剩余H2的混合物,V=V(C3H8)+V剩余(H2)=[5(1-x)L+5x-2×
<x<1,氢气过量,剩余气体的气体体积为C3H8和剩余H2的混合物,V=V(C3H8)+V剩余(H2)=[5(1-x)L+5x-2×![]() 时,即0<x≤
时,即0<x≤![]() ,氢气不足,得到的产物是C3H6或C3H8或二者的混合物,剩余气体的体积等于反应物C3H4的体积,V=V(C3H4)=5(1-x)L,故答案为:0<x≤
,氢气不足,得到的产物是C3H6或C3H8或二者的混合物,剩余气体的体积等于反应物C3H4的体积,V=V(C3H4)=5(1-x)L,故答案为:0<x≤![]() ,V=(5-5x)L;
,V=(5-5x)L;![]() <x<1,V=(10x-5)L。
<x<1,V=(10x-5)L。


科目:高中化学 来源: 题型:
【题目】现有下列两个图象:
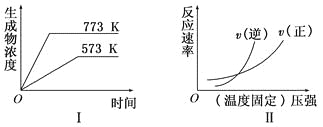
下列反应中符合上述图象的是( )
A. N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0
2SO2(g)+O2(g) ΔH>0
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH>0
C(s)+H2O(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表表示合成氨反应(N2+3H2![]() 2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
|
|
|
|
|
|
200 | 0.153 | 0.815 | 0.899 | 0.954 | 0.988 |
300 | 0.022 | 0.520 | 0.710 | 0.842 | 0.926 |
400 | 0.004 | 0.251 | 0.470 | 0.652 | 0.798 |
分析上表数据,回答下列问题:
(1)200℃、100MPa时,平衡混合物中氨的含量已达0.988,如果继续增大压强______
(填“能”或“不能”)使平衡混合物中氨的含量等于1,理由是:___________________________________________________________________________________________。
(2)欲使平衡混合物中氨的含量增大,则可采取的措施有:____________________。
(3)欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.0.1molL-1CH3COOH溶液加水稀释,CH3COO-数目增多,c(OH-)增大
B.室温下,NaHSO3溶液的pH<7,说明![]() 的电离程度大于其水解程度
的电离程度大于其水解程度
C.酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱。由该理论可知:NaHCO3、H2O、Al(OH)3均可称为酸碱两性物质
D.25℃时0.1molL-1的H2S水溶液中,加入一定量的NaOH溶液,当溶液中存在:c(Na+)=c(S2-)+c(HS-)+c(H2S)时,溶液的主要溶质为Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)反应前A的物质的量浓度是________。
(3)10 s末,生成物D的浓度为________。
(4)A与B的平衡转化率之比为________。
(5)反应过程中容器内气体的平均相对分子质量变化是________(填“增大”、“减小”或“不变”,下同),气体的密度变化是________。
(6)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):①降低温度______;②增大A的浓度________;③恒容下充入氖气_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将amol氮气与bmol氢气的混合气体通入一个固定容积的密闭容器中,发生反应N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,则a值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中氨气体积分数为25%,平衡时氨气的物质的量为________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同)n始∶n平=________。
(4)原气体中a∶b=________。
(5)达到平衡时,N2和H2的转化率之比α(N2)∶α(H2)=________。
(6)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔盐[(NH4)2Fe(SO4)26H2O]是一种浅绿色晶体,广泛应用于电镀工业。为探 究其分解产物,某学习小组利用如图所示装置进行实验。
(查阅资料)隔绝空气加热至500°C时,摩尔盐能完全分解,分解产物中有铁氧化物, 硫氧化物,氨气和水蒸气等。
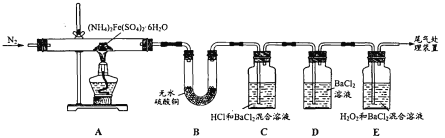
(1)对A装置加热前,先通一段时间N2的目的是_______。
(2)实验开始一段时间后,装置B中的现象为______。
(3)实验中观察到装置D始终无明显现象,装置C中和E中均产生白色沉淀。
①写出E中SO2与H2O2发生反应的化学方程式:_______。
②甲同学根据C中产生白色沉淀现象判断产物中一定含有SO3。请对甲同学的判断作出评价,并说明理由:_____。
(4)实验结束后,装置A中的固体变为红棕色,请补充完整检验该残留固体中是否含 FeO或Fe3O4的实验方案:取A中少量残留固体,加入稀硫酸使其完全溶解,向 溶液中滴加 ________,若观察到 ______,说明残留固体中不含FeO和Fe3O4。(提供的试剂有:NaOH溶液、氯水、硫氰化钾溶液、酸性高锰酸钾溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是一种重要的半导体材料。某工厂利用铝土矿(成分为Al2O3、Ga2O3、Fe2O3等)为原料制备GaN的流程如下图所示:
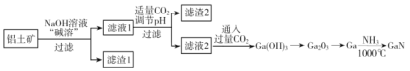
已知:镓与铝同主族,镓的熔点是29.8°C,沸点是2403°C;其氧化物和氢氧化物均为两性化合物;氢氧化物的电离常数如下:
两性氢氧化物 | Al( OH)3 | Ga( OH)3 |
酸式电离常数Ka | 2×10-11 | 1×10-7 |
碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
回答下列问题:
(1)为了提高 “碱溶”效率应采用的措施是__________(回答两种措施)。
(2)滤渣1的成分是_________。
(3)滤液2中通入过量CO2的理由是________(用离子方程式表示)。
(4)流程中利用镓与NH3在1000℃反应生成固体半导体材料 GaN,每生成l molGaN时放出15. 45 kJ热量,写出该反应的热化学方程式________。
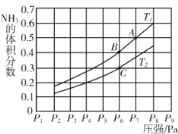
(5)在密闭容器中,充入一定量的Ga与NH3发生反应 ,测得反应平衡体系中NH3的体积分数与压强 P和温度T 的关系曲线如下图所示。图中A 点和C点化学平衡常数的大小关系: KA____KC (填“<”“=”或 “ > ”) , 判断的依据是________。
(6)已知铝土矿中Ga2O3的质量分数为 a%,某工厂使用 w 吨铝土矿经过一系列反应, 反应过程中镓元素的总利用率为 b%能制得________吨氮化镓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com