
已知下列热化学方程式:①Zn(s)+1/2O2(g)===ZnO(s) ΔH1;②Hg(l)+1/2O2(g)===HgO(s) ΔH2。则反应Zn(s)+HgO(s)===Hg(l)+ZnO(s)的ΔH为( )
A.ΔH1-ΔH2 B.ΔH2-ΔH1
C.ΔH1+ΔH2 D.-(ΔH1+ΔH2)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
铁镍蓄电池又称爱迪生电池,放电时的总反应为:
Fe+Ni2O3+3H2O Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-====Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-====Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸式盐NaHY的水溶液显碱性,下列叙述正确的是
( )
A.H2Y的电离方程式:H2Y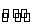 2H++Y2-
2H++Y2-
B.HY-的水解方程式:HY-+H2O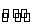 H3O++Y2-
H3O++Y2-
C.该酸式盐溶液中离子浓度关系:[Na+]>[HY-]>[OH-]>[H+]
D.该酸式盐溶液中离子浓度关系:[Na+]>[Y2-]>[HY-]>[OH-]>[H+]
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示,已知Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )

A.只由这四种元素不能组成有机化合物
B.最高价氧化物对应水化物的酸性:W<Z
C.Z的单质与氢气反应的气体产物无色无味
D.X、Y形成的化合物都易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W为短周期元素,原子半径X:99 pm Y:154 pm Z:125 pm W:117 pm,X 、Y、 W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是(双选)( )
| X | ||||
| Y | W |
A.元素Z处于周期表的阴影位置
B.非金属性:X>W
C.X与W形成化合物熔点很高,为离子化合物
D.Y、W的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
向足量的H2SO4溶液中加入100 mL 0.4 mol·L-1 Ba(OH)2溶液,放出的热量是5.12 kJ。向足量的Ba(OH)2溶液中加入100 mL 0.4 mol·L-1 HCl溶液时,放出的热量为2.292 kJ。下列有关反应的热化学方程式中正确的是( )
A.Ba2+(aq)+SO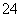 (aq)+2OH-(aq)+2H+(aq)===BaSO4(s)+2H2O(l) ΔH=+128 kJ·mol-1
(aq)+2OH-(aq)+2H+(aq)===BaSO4(s)+2H2O(l) ΔH=+128 kJ·mol-1
B.OH-(aq)+H+(aq)===H2O(l) ΔH=-64 kJ·mol-1
C.Ba2+(aq)+SO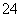 (aq)===BaSO4(s) ΔH=-57.3 kJ·mol-1
(aq)===BaSO4(s) ΔH=-57.3 kJ·mol-1
D.Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-13.4 kJ·mol-1
(aq)===BaSO4(s) ΔH=-13.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
为了探究温度、硫酸铜对锌与稀硫酸反应速率的影响规律,某同学设计如下方案:
| 编号 | 纯锌粉质量 | 0.2 mol·L-1硫酸体积 | 温度 | 硫酸铜固体质量 |
| Ⅰ | 2.0 g | 10.0 mL | 25℃ | 0 |
| Ⅱ | 2.0 g | 10.0 mL | t℃ | 0 |
| Ⅲ | 2.0 g | 10.0 mL | 35℃ | 0.2 g |
| Ⅳ | 2.0 g | 10.0 mL | 35℃ | 4.0 g |
下列推断合理的是( )
A.为了选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,必须控制t=25
B.待测物理量是收集等体积(相同条件)气体所需要的时间,时间越长,反应越快
C.根据该方案,还可以探究硫酸浓度对反应速率的影响
D.根据该实验方案得出反应速率大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Na2CO3和NaHCO3的性质,下列叙述中错误的是( )
|
| A. | 相同温度下,等浓度的Na2CO3和NaHCO3溶液的pH,Na2CO3更大 |
|
| B. | 常温时,Na2CO3的溶解度大于NaHCO3 |
|
| C. | 在酒精灯加热条件下,前者不分解,后者分解 |
|
| D. | 加入澄清石灰水,前者产生沉淀,后者不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
烃分子中若含有双键、三键或环,其碳原子所结合的氢原子数则少于碳原子数对应烷烃所含有的氢原子数,亦具有一定的不饱和度(用Ω表示).下表列出几种烃的不饱和度:
| 有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
| Ω | 1 | 2 | 1 | 4 |
据此下列说法不正确的是( )
|
| A. | 1molΩ=3的不饱和链烃再结合3mol H2,即达到饱和 |
|
| B. |
|
|
| C. | C4H8的不饱和度与C3H6、C2H4的不饱和度不一定相同 |
|
| D. | CH3CH2CH=CH2与环丁烷的不饱和度相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com