
| A. | 若晶体熔融状态下能导电,该晶体一定是离子晶体 | |
| B. | 若晶体熔化时化学键断裂,该晶体一定是原子晶体 | |
| C. | 若晶体中含有非极性分子,该晶体可能有较低的熔沸点 | |
| D. | 若晶体中含有极性共价键,该晶体不可能有很高的熔沸点 |
分析 A、熔融状态下能导电的化合物是离子晶体,熔融状态下能导电的单质是金属;
B、熔化时不需要破坏化学键的是分子晶体,原子晶体、离子晶体、金属晶体熔化时需要破坏化学键;
C、若晶体中含有非极性分子,则该晶体为分子晶体;
D、一般不同非金属元素之间易形成极性键,已知某晶体中含有极性键,则该晶体为化合物,可能是离子化合物、共价化合物.
解答 解:A、熔融状态下能导电的化合物晶体中含有阴阳离子,若是单质,则为金属晶体,故A错误;
B、原子晶体、离子晶体、金属晶体熔化时需要破坏化学键,化学键断裂的晶体不一定是原子晶体,故B错误;
C、若晶体中含有非极性分子,则晶体为分子组成的晶体,为分子晶体,分子晶体熔沸点较低,故C正确;
D、含有极性键的晶体可能是原子晶体,如二氧化硅中含有Si-O极性键,其熔沸点很高,故D错误.
故选:C.
点评 本题考查离子晶体的判断,侧重考查学生分析判断能力,共价化合物和离子化合物可以通过熔融状态是否导电判断,注意不能根据溶解性、熔沸点及水溶液的导电性判断离子晶体,为易错点.


科目:高中化学 来源: 题型:选择题
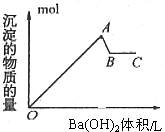
| A. | OA段的反应离子方程式为:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓ | |
| B. | AB段的离子方程式只有:Al(OH)3+OH-→AlO2-+2H2O | |
| C. | A点的沉淀为Al(OH)3和BaSO4的混合物 | |
| D. | B点溶液为KAlO2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b | B. | HA与BOH的电离常数相等 | ||
| C. | 混合溶液中,c(H+)=$\sqrt{{K}_{W}}$mol/L | D. | 混合溶液中,c(H+)+c(B+)═c(OH-)+c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
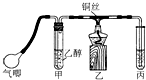 利用如图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物).
利用如图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是极性分子 | |
| B. | 都是共价化合物 | |
| C. | 共价分子间的作用力都比化学键弱 | |
| D. | 溶于水的共价分子都能产生自由移动的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制备乙烯时,产生的气体使溴水褪色,能证明有乙烯生成 | |
| B. | 除去溴苯中的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 | |
| C. | 加热NaOH和少量溴乙烷的混合液后滴加硝酸银,可生成浅黄色沉淀 | |
| D. | 制取硝基苯时,试管中先加入浓H2SO4,再逐滴滴入浓HNO3和苯,振荡混合均匀后,保持55℃水浴加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| B. | “硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| C. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| D. | 华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com