
【题目】在不同条件下,分别测得反应2SO2(g)+O2(g)![]() 2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
A. υ(SO2)=4 mol·L-1·min-1B. υ(O2)=3 mol·L-1·min-1
C. υ(SO2)=0.1 mol·L-1·s-1D. υ(O2)=0.1 mol·L-1·s-1
科目:高中化学 来源: 题型:
【题目】有关下列四个图象的说法中正确的是( )
A.①表示等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,其产生的氢气总体积(V)与时间(t)的关系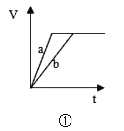
B.②表示合成氨反应中,每次只改变一个条件,得到的反应速率v与时间t的关系,则t3时改变的条件为增大反应容器的体积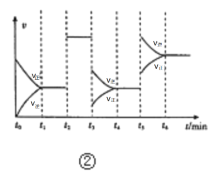
C.③表示其它条件不变时,反应4A(g)+3B(g)![]() 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化情况,则D一定是气体
2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化情况,则D一定是气体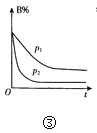
D.④表示恒温恒容条件下发生的可逆反应2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态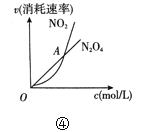
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量
B. 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态
C. 热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据
D. 凡是化合反应都是放热反应,分解反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据合成氨反应的能量变化示意图,下列有关说法正确的是( )
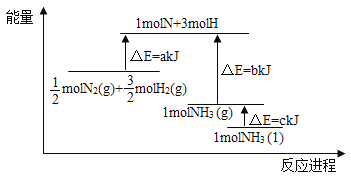
A. 若合成氨反应使用催化剂,反应放出的热量增多
B. 断裂0.5moIN2(g)和1.5molH2(g)中所有的化学键释放akJ热量
C. 2NH3(l)= N2(g)+3H2(g) △H=2(b+c-a) kJ/mol
D. N2(g)+3H2(g)=2NH3(g) △H=-2(a-b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(molL﹣1s﹣1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示的关系:υ(B)=3υ(A); 3υ(C)=2υ(B)。则此反应可表示为( )
A. 2A+3B![]() 2CB. A+3B
2CB. A+3B![]() 2C
2C
C. 3A+B![]() 2CD. A+B
2CD. A+B![]() C
C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读短文,回答问题。
锂离子电池是一种生活中常见的二次电池,常用于手机、笔记本电脑、电动车中。它主要依靠Li+在正极材料(LixCOO2)和负极材料(石墨)之间往返嵌入和脱嵌来工作。低温时,由于电解液粘度增大,电池中锂离子的迁移能力下降。低温充电时石墨嵌锂速度降低,Li+来不及嵌入石墨中形成LixC,便得到电子被还原,容易在负极表面析出金属锂,降低电池容量,影响电池安全。上海复旦大学开发了一款新型锂离子电池,其放电的工作原理如图1所示。该电池不仅在-40℃下放电比容量没有衰降,甚至在-70℃下该电池的容量保持率也能够达到常温的70%左右,极大地拓展了电池的应用范围。复旦大学团队采用凝固点低、可在极端低温条件下导电的乙酸乙酯基电解液,并采用不需要将锂离子嵌入到电极中即可完成充、放电的有机物电极,避免了低温条件下嵌入过程变慢。请依据文章内容回答下列问题。
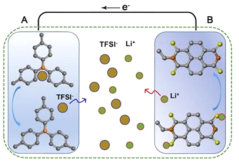
(1)判断下列说法是否正确_________(填“对”或“错”)。
①新型锂离子电池有望在地球极寒地区使用。
②在传统锂离子电池中,金属锂是负极材料。
③若新型锂离子电池在常温下的放电比容量为99mAh·g-1,则其在-40℃下的放电比容量为99mAh·g-1。
(2)新型锂离子电池放电时,正极是_________(填“A”或“B”)。
(3)下列关于该新型锂离子电池可耐低温原因的推测中,不正确的是_________(填字母)。
a.采用与传统不同的有机物电极
b.乙酸乙酯基电解液的凝固点低
c.锂离子不需要在正负极间移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁粉具有平肝镇心,消痈解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组探究用氢气和碳酸亚铁制取铁粉并检验反应产物,实验装置如图。下列说法不正确的是
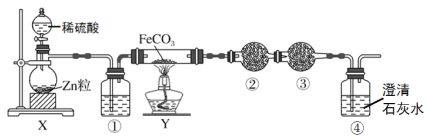
A.通过调节分液漏斗的活塞以控制①中气泡产生快慢
B.装置①的作用是干燥氢气
C.装置②、③中的药品分别是无水硫酸铜、碱石灰
D.加热装置Y前,应先让X反应一段时间,排除装置中的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中充入气体A和B,发生A(g)+B(g)C(g)+2D(g) ΔH,所得实验数据如表。下列说法不正确的是
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(A) | n(B) | n(C) | ||
① | 300 | 0.40 | 0.10 | 0.090 |
② | 500 | 0.40 | 0.10 | 0.080 |
③ | 500 | 0.20 | 0.05 | a |
A.ΔH>0
B.500 ℃该反应的平衡常数K=0.16 mol·L-1
C.③中达到平衡时,A的转化率大于20%
D.5min末测得①中n(C)=0.050 mol,则0到5min内v(D)=0.02mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是一种重要的有机化工原料,用于制丙烯腈、环氧丙烷、丙酮等。回答下列问题:
(1)已知:
I.C3H8(g)![]() C3H6(g)+H2(g) △H1=+124kJ/mol
C3H6(g)+H2(g) △H1=+124kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
则丙烷氧化脱氢制丙烯反应2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
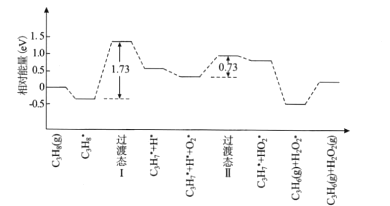
①该反应历程中决速步骤的能垒(活化能)为_________eV,该步骤的化学方程式为________
②请补充该历程之后可能发生的化学反应方程式_____________
(3)已知丙烷氧化脱氢容易发生副反应:2C3H8(g)+O2(g)![]() 3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=
3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=![]() ×100%]
×100%]
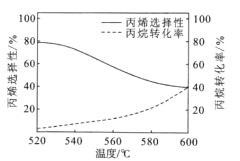
①丙烯的选择性随着温度的升高而降低的可能原因有_________
②在反应温度为600℃,将C3H8与O2以体积比为1:1充入刚性容器中,达到平衡时,丙烷的转化率为40%,丙烯的选择性也为40%,体系总压强为pkPa,则氧气的转化率![]() (O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
(O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com