
下列水解离子方程式中,正确的是( )
A.Fe3++3H2O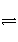
 Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.Br-+H2O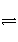
 HBr+OH-
HBr+OH-
C.CO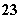 +2H2O
+2H2O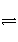
 H2CO3+2OH-
H2CO3+2OH-
D.NH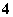 +2H2O
+2H2O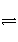
 NH3·H2O+H3O+
NH3·H2O+H3O+
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推测正确的是 ( )
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl、HBr、HI的热稳定性依次增强
D.若M+和R2-的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
B.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol--1,则氢气的燃烧热为241.8 kJ·mol-1
C.已知2C(s)+2O2(g)=2CO2(g) △H=a、2C(s)+O2(g)=2CO(g) △H=b,则a>b
D.已知P (白磷,s)=P (红磷,s) △H<0,则白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状态下,气态分子断开l mol化学键的焓变称为键焓。已知H-H、H-O
和O-O键的键焓ΔH分别为436 kJ/mol、463 kJ/mol和495kJ/mol。下列热化学方程式正确的是
A.H2O (g)= H2(g)+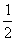 O2(g); ΔH= -485 kJ/mol
O2(g); ΔH= -485 kJ/mol
B.H2O (g)=H2(g)+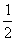 O2(g); ΔH==+485 kJ/mol
O2(g); ΔH==+485 kJ/mol
C.2H2(g)+ O2 (g)= 2H2O(g) ΔH = +485 kJ/mol
D.2H2(g)+ O 2(g)=2H2O(g) ΔH = -485 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
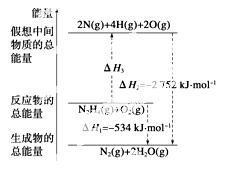
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol
化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则
断裂1 mol N—H键所需的能量(kJ)是 ( )
A.194 B.391 C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.碳酸的电离:H2CO3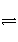
 2H++CO
2H++CO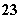
B.将金属钠加入水中:2Na+2H2O===2Na++2OH-+H2↑
C.硫化钠水解:S2-+2H2O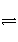
 H2S↑+2OH-
H2S↑+2OH-
D.向氯化铝溶液中加入过量的烧碱溶液:Al3++3OH-===Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
浓度为0.1 mol·L-1的8种溶液:
①HNO3 ②H2SO4 ③HCOOH ④Ba(OH)2 ⑤NaOH
⑥CH3COONa ⑦KCl ⑧NH4Cl溶液pH由小到大的顺序是____________________(填写编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将一小块钠投入到CuCl2溶液中,观察到的现象是( )
A.钠溶解,有铜析出并有气体产生
B.只有气体产生
C.只有沉淀产生
D.既有气体产生,又有蓝色沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是
A .单质钠的密度比钾的密度小 B.Na+和K+常用作氧化剂
.单质钠的密度比钾的密度小 B.Na+和K+常用作氧化剂
C.钠和钾都是短周期元素 D.钠和钾的合金[ω(K)=50%~80%]在室温下呈液态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com