
下列说法正确的是( )
A. 硫酸钡不溶于水,所以硫酸钡是非电解质
B. 二氧化碳溶于水可以导电,所以,二氧化碳是电解质
C. 固态磷酸是电解质,所以磷酸在熔化时或溶于水时都能导电
D. 液态氯化氢不能导电,但氯化氢是电解质
科目:高中化学 来源:2017届河北省高三上期末化学试卷(解析版) 题型:选择题
已知2H→H2放出437.6 kJ的热量,下列说法正确的是( )
A.氢气分子内每个氢原子都达到了8电子稳定结构
B.1 mol H2的能量比2 mol H的能量低
C.1 mol H2离解成2 mol H要放出437.6 kJ热量
D.氢原子不如氢分子活泼
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团第二师华山中学高二上学期期末考试化学试卷(解析版) 题型:简答题
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
温度(T) | K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
从上表可推断,反应①是________(填“放”或“吸”)热反应。
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q3的平衡常数为K3
CO(g)+H2O(g) ΔH=Q3的平衡常数为K3
Ⅰ.根据反应①与②推导出Q1、Q2、Q3的关系式Q3=________。根据反应①与②推导出K1、K2、K3的关系式K3=____________;可推断反应③是________(填“放”或“吸”)热反应。
Ⅱ.要使反应③在一定条件下建立的平衡右移,可采取的措施有________。
A.缩小容器体积
B.降低温度
C.使用合适的催化剂
D.设法减少CO的量
E.升高温度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团第二师华山中学高二上学期期末考试化学试卷(解析版) 题型:选择题
“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求。你认为下列行为不符合这个要求的是( )
A. 将煤转化成气体燃料可以有效地减少“温室效应”的气体产生
B. 加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用
C. 研制开发以水代替有机溶剂的化工涂料
D. 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高一下学期第一次月考化学试卷(解析版) 题型:选择题
某溶液含有①NO3-②HCO3-③SO32-④CO32-⑤SO42-等五种离子,向其中加入少量的Na2O2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积的变化)( )
A. ① B. ①②④ C. ①③⑤ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列有关实验操作、发生的现象、解释或结论都正确的是( )
选项 | 实验操作 | 产生的现象 | 解释或结论 |
A | 向Na2SO3溶液中逐滴加入硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | 产生的BaSO3是难溶于水的沉淀 |
B | 将SO2通入滴有酸性高锰酸钾溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
C | 常温下铜片插入硝酸中 | 产生红棕色气体 | 常温下铜和硝酸一定产生NO |
D | 向某溶液中加入NaHCO3 | 产生白色沉淀 | 该溶液可能原来含有氢氧化钡 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省淮北市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中,不正确的是( )
A. 胶体与溶液的本质区别是分散质颗粒的大小不同
B. 氯化铁溶液可应急止血,利用的是胶体的聚沉
C. 溶液是电中性的,胶体是带电的
D. 将稀硫酸逐滴加入氢氧化铁胶体中,开始时产生沉淀,继续滴加时沉淀又溶解
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三12月月考化学卷(解析版) 题型:实验题
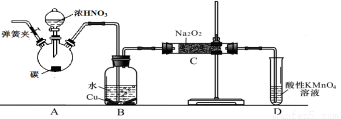
亚硝酸钠是重要的防腐剂。某化学兴趣 小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
查阅资料:①HN O2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
O2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠。
(1)A中反应的化学方程式是 。
(2)B中观察的主要现象是 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的操作是 。
(4)经检验C产物中亚硝酸钠含量较少。
a.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。
生成碳酸钠的化学方程式是 。为排除干扰甲在B、C装置间增加装置E,E中盛放的试剂应是 (写名称)。
b.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 。
(5)实验经改进后可制得较纯亚硝酸钠,下列说法正确的是 。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸溶液pH>1
c.已知亚硝酸电离平衡常数为Ka;亚硝酸根水解常数为Kh;水的离子积为Kw;则三者关系为:Ka·Kh=Kw
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试化学试卷(解析版) 题型:选择题
一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5 mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com