
【题目】室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关叙述正确的是

A.pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.向W点所表示的1.0L溶液中通人0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-)
C.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)-
D.pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l
【答案】C
【解析】
试题室温条件下,在醋酸、醋酸钠混合溶液中,醋酸的浓度越大溶液的pH越小,故图中实线表示c(CH3COO-),虚线表示c(CH3COOH)。A、由图像知pH=5.5的溶液中:c(CH3COO-)>c(CH3COOH)> c(H+)>c(OH-),错误;B、W点所表示的溶液中c(CH3COOH)=c(CH3COO-)=0.05mol.L-1,向1.0L溶液中通人0.05molHCl气体所得溶液为醋酸和氯化钠的混合液,根据电荷守恒知:c(H+)=c(CH3COO—)+c(OH-),错误;C、根据电荷守恒知醋酸、醋酸钠混合溶液中c(Na+)+c(H+)= c(CH3COO-)+c(OH)-,根据图像知W点所表示的溶液中c(CH3COO-)= c(CH3COOH),则c(Na+)+c(H+)=c(CH3COOH)+c(OH-),正确;D、根据电荷守恒知醋酸、醋酸钠混合溶液中c(Na+)+c(H+)= c(CH3COO-)+c(OH)-,又c(CH3COOH)+c(CH3COO-)=0.lmol.L-1,则c(CH3COO-)=0.lmol.L-1- c(CH3COOH),故pH=3.5的溶液中:
c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol.L-l,错误。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO。实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生。

(1)铜与稀硝酸反应的化学方程式为_________________。
(2)NO是大气污染物之一。目前有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨气把NO还原为氮气和水。该反应的化学方程式为4NH3+6NO![]() 5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为__________。
5N2+6H2O,每有5 mol N2生成,氧化产物与还原产物的物质的量之比为__________。
(3)若将上述稀硝酸换成浓硝酸,其生成的气体通入水中,该气体与水反应的化学方程式为______________________________________________。
(4)①写出实验室由NH4Cl和Ca(OH)2加热制取氨气的化学方程式__________。
②进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两个重要性质分别是________________________、___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,2002年10月26日俄罗斯特种部队在解救人质时,除使用了非致命武器芬太奴外,还作用了一种麻醉作用比吗啡强100倍的氟烷,已知氟烷的化学式为C2HClBrF3,则沸点不同的上述氟烷有
A. 3种B. 4种C. 5种D. 6种
查看答案和解析>>
科目:高中化学 来源: 题型:
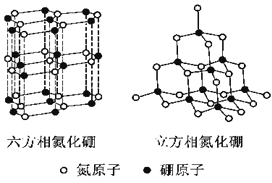
【题目】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。
(1)基态硼原子的电子排布式为 。
(2) 关于这两种晶体的说法,正确的是 (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石墨相似却不导电,原因是 。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为 。该晶体的天然矿物在青藏高原在下约300km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mol NH4BF4含有 mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、Q 、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题:
(1)X元素在周期表中的位置是_______________,它的外围电子的电子排布图为 _______________________________,P元素属于_______区元素。
(2)XZ2分子的空间构型是________ ,YZ2分子中Y的杂化轨道类型为_________ ,相同条件下两者在水中的溶解度较大的是__________(写分子式),理由是_____________________。
(3)含有元素N的盐的焰色反应为____色,许多金属盐都可以发生焰色反应,其原是________________________
(4)元素M与元素Q形成晶体结构如图1所示,设其晶胞边长为a pm,该化合物的摩尔质量为Dg/mol。求该晶胞密度的计算式为_______________g/cm3
(5)三聚氰胺是一种含氮化合物,其结构简式如图2所示。 三聚氰胺分子中氮原子轨道杂化类型是______, 1 mol三聚氰胺分子中 σ键的数目为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有6个N﹣H键断裂
②v(H2)=0.6molL﹣1min﹣1,v(NH3)=0.4molL﹣1min﹣1
③保持其他条件不变时,体系压强不再改变;
④NH3、N2、H2的体积分数都不再改变;
⑤恒温恒容时,混合气体质量保持不变。
A. ②③④ B. ①②④ C. ①③④ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cu片放入0.1 mol·L1 FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+)∶c(Fe2+)=2∶1,则Cu2+与原溶液中的Fe3+的物质的量之比为( )
A. 4∶1 B. 1∶4 C. 1∶6 D. 6∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com