
��֪��CO2(g)+3H2(g)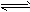 CH3OH(g)+H2O(g) ��H="-49.0" kJ/mol��һ�������£������Ϊ1L���ܱ������г���1 mol CO2��3mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯��������ͼ��ʾ�����������У���ȷ����
CH3OH(g)+H2O(g) ��H="-49.0" kJ/mol��һ�������£������Ϊ1L���ܱ������г���1 mol CO2��3mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯��������ͼ��ʾ�����������У���ȷ����
| A�������¶���ʹƽ��������Ӧ�����ƶ� |
| B���ӷ�Ӧ��ʼ��ƽ�⣬v(H2)=0.075mol��L-1��min-1 |
| C��3 minʱ��V(CO2)�� = V(CH3OH)�� |
| D����Ӧ�ﵽƽ��״̬ʱ��CO2��ƽ��ת����Ϊ75% |
 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������н��з�ӦM(g)��N(g)  Y(g)��2Z(?)������Y��ƽ�������е�����������Y%)��ͬ�¶ȡ�ѹǿ��������ʱ��ı仯��ͼ��ʾ��������������ȷ����
Y(g)��2Z(?)������Y��ƽ�������е�����������Y%)��ͬ�¶ȡ�ѹǿ��������ʱ��ı仯��ͼ��ʾ��������������ȷ����
| A������ӦΪ���ȷ�Ӧ��Z������ |
| B������ӦΪ���ȷ�Ӧ��Z�ǹ����Һ�� |
| C������ӦΪ���ȷ�Ӧ��Z������ |
| D������ӦΪ���ȷ�Ӧ��Z�ǹ����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ݻ��ɱ���ܱ������д������·�Ӧ��2A(g)��B(g) 3C(g) ��H��0��ij�о�С���о���������������ʱ��ֻ�ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����( )
3C(g) ��H��0��ij�о�С���о���������������ʱ��ֻ�ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����( )
| A��ͼ���ʾ����t1ʱ�������¶ȶԷ�Ӧ���ʵ�Ӱ�� |
| B��ͼ���ʾ��һ����t1ʱ�̼��������Է�Ӧ���ʵ�Ӱ�� |
| C��ͼ���ʾ�����¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ� |
| D��ͼ���ʾ���Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ����������������ԭ�����͵���
| A�����Ṥҵ�У�����O2��Ũ�����������SO2��ת���� |
B����2HI H2+I2ƽ����ϵ����ѹǿʹ��ɫ���� H2+I2ƽ����ϵ����ѹǿʹ��ɫ���� |
| C������ơ��ƿ��ƿ�����̷��������ĭ |
| D�����з�̪�İ�ˮ��Һ���ʵ�������Һ���������ӷ�������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ҵ�Ͽ����úϳ�����CO��H2�Ļ�����壩�����״�����֪��
CO(g)+2H2(g) CH3OH(g) ��H=��92.9kJ/mo1
CH3OH(g) ��H=��92.9kJ/mo1
һ�������£��÷�Ӧ��һ����̶����ܱ������дﵽƽ�⡣����˵����ȷ����
| A���÷�Ӧ�ġ�S<0 |
| B���÷�Ӧ���κ��¶��¾����Է����� |
| C���������г�������He��ƽ��������Ӧ�����ƶ� |
| D�������¶�ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڷ�ӦA2+3B2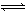 2C��˵�����±�ʾ�Ļ�ѧ��Ӧ����������
2C��˵�����±�ʾ�Ļ�ѧ��Ӧ����������
A��v (B2)="1.8" mol��L-1��min-1 B��v (A2)="0.4" mol��L-1��s-1
C��v (C)="0.6" mol��L-1��s-1 D��v (B2)="0.42" mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
NO2��������ƽ�⣺2NO2(g)  N2O4(g)+Q��Q>0�� �ڲⶨNO2����Է�������ʱ�����������²ⶨ�����ӽ�����ֵ����
N2O4(g)+Q��Q>0�� �ڲⶨNO2����Է�������ʱ�����������²ⶨ�����ӽ�����ֵ����
| A���¶�130�桢ѹǿ3.03��105 Pa | B���¶�25�桢ѹǿ1.01��105 Pa |
| C���¶�130�桢ѹǿ5.05��104 Pa | D���¶�0�桢ѹǿ5.05��104 Pa |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ĸ���ͬ�������н��кϳɰ��ķ�Ӧ��������������ͬʱ���ڲⶨ�Ľ�����ж����ɰ�������������
| A��v (N2)=0��05mol��L��1��s��1 | B��v (H2)=0��3mol��L��1��min��1 |
| C��v (N2)=0��2 mol��L��1��min��1 | D��v (NH3)=0��3 mol��L��1��min��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ�У�������ɳ����ԭ�������͵���
| A����H2(g)��I2(g)��HI(g)��ɵĻ������ƽ����ϵ��ѹ����ɫ���� |
| B�����õ���ˮ�����ϡ���� |
| C����FeCl3��Һ�м������۷�ֹ�������� |
| D���������������SO2��O2��Ӧ��SO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com