
【题目】可逆反应aA(g)+bB(g) ![]() cC(g)+dD(g) ΔH,同时符合下列两图中各曲线规律的是( )
cC(g)+dD(g) ΔH,同时符合下列两图中各曲线规律的是( )
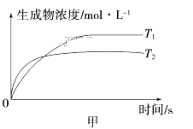
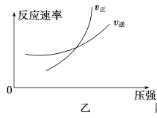
A.a+b>c+d T1>T2 ΔH>0
B.a+b>c+d T1<T2 ΔH<0
C.a+b<c+d T1>T2 ΔH>0
D.a+b<c+d T1<T2 ΔH<0
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】呋喃甲酸( )俗名糠酸,其在塑料工业中可用作增塑剂、热固性树脂等,在食品工业中可用作防腐剂,也可用作涂料添加剂、医药。呋喃甲酸可由呋喃甲醛制备,其制备原理如下所示:
)俗名糠酸,其在塑料工业中可用作增塑剂、热固性树脂等,在食品工业中可用作防腐剂,也可用作涂料添加剂、医药。呋喃甲酸可由呋喃甲醛制备,其制备原理如下所示:
反应1:
反应2:
已知:
Ⅰ.反应1是放热反应;
Ⅱ.乙醚的沸点是34.6 ℃,易挥发,遇明火易燃,其蒸气可使人失去知觉;
Ⅲ.呋喃甲酸的溶解度随温度的升高而升高,且升温过程中溶解度变化较大。
(实验步骤)
向三颈烧瓶中加入16.4 mL(约0.2 mol)呋喃甲醛,控制温度在8~12℃下滴加20 mL 40% NaOH溶液,并搅拌回流半小时。向反应混合物中加水使其恰好溶解,加入乙醚分离呋喃甲醇和呋喃甲酸盐,向水层中慢慢滴加浓盐酸,搅拌,析出结晶,并通过进一步提纯得到精产品9.5 g。


(1)若用如图装置作为反应1的发生装置,图中有一处明显错误的地方是__________。
(2)步骤①中,为控制反应温度在8~12℃,可采取的措施有:
①________________________________;②_______________________________。
(3)操作1的名称为________,要用到的玻璃仪器有________。
(4)在对乙醚层进行分离时,用下图中的________(填字母代号)装置更好,与另一装置相比,该装置具有以下优点:

①______________________;②__________________。
(5)经过结晶得到的粗呋喃甲酸若要进一步提纯,要经过热水溶解→活性炭脱色→蒸发浓缩→____→_____→抽滤→洗涤→干燥。
(6)呋喃甲酸的产率为____(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,向某恒容密闭容器中充入![]() 和
和![]() 发生反应:
发生反应:![]() ,反应历程与能量的变化如图所示,下列说法错误的是 ( )
,反应历程与能量的变化如图所示,下列说法错误的是 ( )
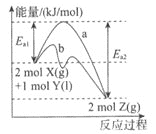
A.Y的质量不变时,该反应达到平衡状态
B.反应达到平衡时,放出的热量小于![]()
C.曲线b为加入催化剂时该反应的反应历程图
D.其他条件不变,平衡后再充入![]() ,达到新平衡时,Z的体积分数减小
,达到新平衡时,Z的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、R、Y、Z、M为五种短周期元素,其原子半径和最外层电子数之间的关系如图1所示。R位于第三周期,Z、M的最高价氧化物对应的水化物分别为甲、乙。常温下,0.1molL﹣1的甲溶液的pH为1.回答下列问题:

(1)R的某种氧化物为淡黄色固体,写出该氧化物的一种用途:_____。
(2)单质Y与乙的浓溶液共热产生两种无色气体,现用图2的装置检验这两种气体。B中试剂名称为_____;C中酸性KMnO4溶液的作用为_____。若C中溶液颜色褪尽,D中澄清石灰水变浑浊,则此现象不能证明产物中_____(化学式)气体的存在。
(3)写出铜和甲的稀溶液反应的离子方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯容易发生聚合生成二聚体,该反应为:2![]()
![]()
![]() ΔH<0。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是
ΔH<0。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是

A.T1<T2
B.a点的正反应速率大于b点的逆反应速率
C.达平衡后,T1温度下环戊二烯的浓度大于T2温度下环戊二烯的浓度
D.反应开始至b点时,双环戊二烯平均速率约为:0.45molL-1h-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式不正确的是
A.用石墨电极电解饱和食盐水:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.明矾可以做净水剂:Al3++3H2O=Al(OH)3↓+3H+
C.向铁制器具上电镀铜,阴极的电极反应为:Cu2++2e-=Cu
D.向氢氧化镁浊液中滴入酚酞溶液,溶液变红:Mg(OH)2(s)Mg2+(aq)+2OH-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
![]() 离子化合物含离子键,也可能含极性键或非极性键
离子化合物含离子键,也可能含极性键或非极性键
![]() 硫酸的酸性大于碳酸的酸性,所以非金属性
硫酸的酸性大于碳酸的酸性,所以非金属性![]()
![]() 含金属元素的化合物不一定是离子化合物
含金属元素的化合物不一定是离子化合物
![]() 由非金属元素组成的化合物一定是共价化合物
由非金属元素组成的化合物一定是共价化合物
![]() 熔融状态能导电的化合物是离子化合物
熔融状态能导电的化合物是离子化合物
![]() 由分子组成的物质中一定存在共价键
由分子组成的物质中一定存在共价键
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,已知E1=+134kJ·mol-1、E2=+368kJ·mol-1,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。请写出NO2和CO反应的热化学方程式:________。

(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
a:2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
b:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
c:H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com