
某课外活动小组,称取了10.8g青铜进行研究,他们 将青铜放入过量稀盐酸中,得到SnCl2和PbCl2的混合溶液,收集到的气体在101kPa下,冷却到25℃是272mL,冷却到10℃是267mL。已知该青铜合金中铜的质量分数是84.8%,试求该青铜合金中锡、铅的质量分数。
将青铜放入过量稀盐酸中,得到SnCl2和PbCl2的混合溶液,收集到的气体在101kPa下,冷却到25℃是272mL,冷却到10℃是267mL。已知该青铜合金中铜的质量分数是84.8%,试求该青铜合金中锡、铅的质量分数。
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源:2017届湖北省孝感市高三上第一次统考化学试卷(解析版) 题型:填空题
一定条件下发生反应:M2(?)+2R2(g) M2R4(g)
M2R4(g)
(1)在容积一定、温度一定的密闭容器中加入一定量M2和R2,反应过程中测得气体的平均相对分子质量随时间的变化如下图a所示,则对M2物质的状态判断正确的是______(填序号)
A.只能为气体 B.只能为固体 C.既可能为固体,也可能为气体
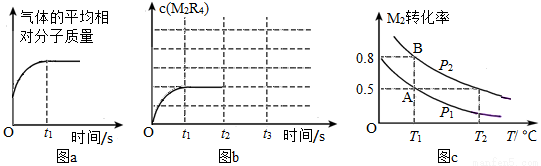
(2)若在t2时,维持温度不变将容器体积迅速压缩为原来的一半,t3时达到新的平衡。在上图b中画出t2后c(M2R4)的变化曲线。
(3)若M2为气态,根据上图c回答下列问题:
①该反应为________(填“放”或“吸”)热反应;P2________P1(填“>”或“<”)。
②在一容积可变的密闭容器中充入10mo1M2气体和30mo1R2气体,当达到平衡状态A时,容器容积为20L。如反应开始时仍充入10mo1M2和30mo1R2,则在平衡状态B时,容器容积V (B)=____________L。
③在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生该反应(起始温度和起始容器容积均相同),有关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1 mol M2、2 mol R2 | 1 mol M2R4 | 1 mol M2R4 |
平衡时容器体积 | V (甲) | V (乙) | V (丙) |
反应的平衡常数K | K(甲) | K(乙) | K(丙) |
平衡时M2R4的浓度(mol·L-1) | c (甲) | c (乙) | c(丙) |
平衡时M2R4的反应速率(mol·L-1·min-1) | v (甲) | v (乙) | v (丙) |
则下列说法正确的是_________。
A.V (甲)>V (丙) B.K(乙)>K(丙) C.c (乙)>c (甲) D.v (甲)=v (丙)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:实验题
某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(图中铁架台等夹持仪器均已略去):
Ⅰ、实验装置如图所示
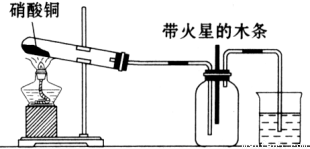
⑴硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气。写出该反应的化学方程式: 。
⑵当集气瓶中充满红棕色气体时,木条复燃。有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
Ⅱ、实验装置如图所示
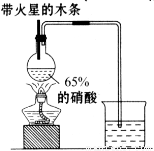
⑴写出浓硝酸受热分解的化学方程式: 。
⑵实验开始后木条上的火星逐渐熄灭,有的同学提出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:选择题
溶液、胶体和浊液这三种分散系的根本区别是
A.是否有丁达尔现象 B.分散质粒子的大小
C.能不能通过滤纸或半透膜 D.是否均一、稳定、透明
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:选择题
脍炙人口的“千锤万凿出深山,烈火焚烧若等闲;粉身碎骨浑不怕,要留清白在人间。”是明代名臣于谦的名作《石灰吟》。这四句中没有涉及化学变化的是
A.千锤万凿出深山 B.烈火焚烧若等闲
C.粉身碎骨浑不怕 D.要留清白在人间
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市钦州港区高一12月月考化学卷(解析版) 题型:推断题
已知有以下物质相互转化。
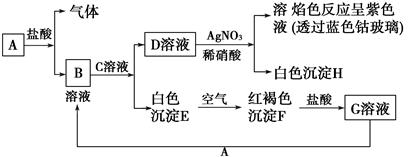
试回答:
(1)写出B的化学式__________,D的化学式__________。
(2)写出由E转变成F的化学方程式_______________________。
(3)写出用KSCN鉴别G现象___________;向G溶液加入A的有关离子反应方程式___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市钦州港区高一12月月考化学卷(解析版) 题型:选择题
在Al2(SO4)3、K2SO4和明矾的混合溶液中,如果c(SO42-)等于0.2mol/L,当加入等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混合溶液中K+的物质的量浓度为
A.0.2mol/L B.0.25mol/L C.0.45mol/L D.0.225mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市高新区高一12月月考化学试卷(解析版) 题型:实验题
某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质。请回答下列问题:
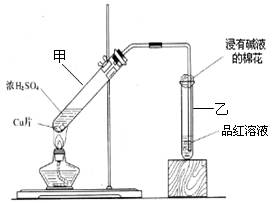
(1)试管乙中发生的现象是 ,该现象能说明产生的气体具有 性。
(2)写出 试管甲中所发生反应的化学方程式,并标明电子转移方向和数目。
试管甲中所发生反应的化学方程式,并标明电子转移方向和数目。
(3)试管乙口部浸有碱液的棉花的作用是 。
(4)SO 2 的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水V L,加入0.5 mol/L的Ba(OH) 2 溶液至不再产生沉淀时,恰好消耗20.00 mL Ba(OH) 2 溶液。请计算:
①该雨水中共溶解标准状况下SO 2 的体积多少mL?
②若生成沉淀物的质量为2.25 g,求出沉淀物的组成。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期末化学卷(解析版) 题型:选择题
如图,a、b、d均为石墨电极,c为Mg电极,通电进行电解(电解液足量),下列说法正确的是
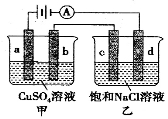
A.向甲中加入适量Cu(OH)2,溶液组成可以恢复
B.电解一段时间,乙溶液中会产生白色沉淀
C.当b极增重3.2g时,d极产生的气体体积为1.12L
D.甲中b极上的电极反应式为:4OH--4e-=O2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com