
【题目】已知五种短周期元素aX、bY、cZ、dR、eW存在如下关系:① X、Y同主族,R、W同主族 ②![]() ;a+b=
;a+b=![]() (d+e);
(d+e);![]() =c-d,下列有关说法不正确的是
=c-d,下列有关说法不正确的是
A.原子半径比较:r(W)>r(Z)>r(Y) >r(R)
B.X和Y形成的化合物中,阴阳离子的电子层相差1层
C.W的最低价单核阴离子的失电子能力比R的强
D.Z、Y最高价氧化物对应的水化物之间可以相互反应
【答案】A
【解析】
根据R,W 同主族,并且原子序数R为W的一半可知,R为O元素,W为S元素;根据![]() 可知,X和Y的原子序数和为12,又因为X和Y同主族,所以X和Y一个是H元素,一个是Na元素;考虑到
可知,X和Y的原子序数和为12,又因为X和Y同主族,所以X和Y一个是H元素,一个是Na元素;考虑到![]() ,所以X为H元素,Y为Na元素,那么Z为Al元素。
,所以X为H元素,Y为Na元素,那么Z为Al元素。
A.W,Z,Y,R分别对应S,Al,Na,O四种元素,所以半径顺序为:r(Y)>r(Z)>r(W)>r(R),A项错误;
B.X与Y形成的化合物即NaH,H为-1价,H-具有1个电子层,Na为正一价,Na+具有两个电子层,所以,B项正确;
C.W的最低价单核阴离子即S2-,R的即O2-,还原性S2-更强,所以失电子能力更强,C项正确;
D.Z的最高价氧化物对应水化物为Al(OH)3,Y的为NaOH,二者可以反应,D项正确;
答案选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】依据A~E几种烃分子的示意图或结构填空。
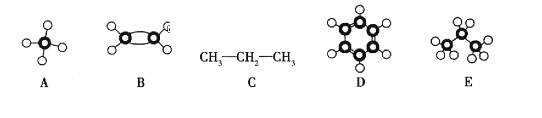
(1)E的分子式是_____________________。
(2)属于同一物质的是___________(填序号)。
(3)与C互为同系物的是___________(填序号)。
(4)等物质的量的上述烃完全燃烧时消耗![]() 最多的是___________(填序号,下同);等质量的上述烃完全燃烧时消耗
最多的是___________(填序号,下同);等质量的上述烃完全燃烧时消耗![]() 最多的是_____________。
最多的是_____________。
(5)在120℃,![]() 下,A和C分别与足量
下,A和C分别与足量![]() 混合点燃,完全燃烧后恢复至初始状态,气体体积没有变化的是______________(填序号)。
混合点燃,完全燃烧后恢复至初始状态,气体体积没有变化的是______________(填序号)。
(6)C的某种同系物的分子式为![]() ,其一氯代物只有一种,该烃的结构简式为______________________。
,其一氯代物只有一种,该烃的结构简式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D、E五种有机物的有关信息:
A | B | C | D | E |
①能使溴的四氯化碳溶液褪色; ②比例模型为: ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为: | 分子式为C2H6O,能与E酯化 | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为: |
根据表中信息回答下列问题:
(1)A到E中,属于烃的是__________(填字母);写出A与溴水反应的化学方程式__________。
(2)B具有的性质是__________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水小 ⑤可使酸性高锰酸钾溶液和溴水均褪色
(3)写出C、D 结构简式:__________、__________。
(4)E 中含氧官能团的名称__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家通过测量SiO2中的26Al和10Be两种元素的比例确定“北京人”年龄,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)写出Be的核外电子排布式_______________。Be所在的周期中,最外层有2个未成对电子的元素的符号是_______、_________。
(2)写出Al的最外层电子轨道表示式__________________。铝原子核外有_______种运动状态不同的电子;铝原子核外有_______中能量不同的电子。
(3)比较Al3+、S2-和Cl-半径由大到小的顺序_________________________;这3种元素最高价氧化物对应的水化物中酸性最强的是___________(写化学式)。
(4)铝元素最高价氧化物与氢氧化钠溶液反应的化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.硫酸铜溶液中加过量的氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
B.用食醋检验牙膏中碳酸钙的存在:CaCO3+2H+=Ca2++CO2↑+H2O
C.将去膜的铝片投入到NaOH溶液中:2Al+2OH—+6H2O=2[Al(OH)4]— +3H2↑
D.用碘化钾淀粉溶液检验亚硝酸钠中NO2-的存在:NO2-+2I-+2H+=NO↑+I2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 1 L 1 mol/L 的 CH3COOH 溶液中 CH3COO-为 NA个
B. 标况下 22.4 L NO 和 11.2 L O2 反应后,气体分子总数为 NA个
C. 1 L 0.1 mol/L 的 Na2SO3 溶液中离子总数大于 0.3NA
D. H2和 O2反应生成 NA个 H2O(l)和 NA个 H2O(g)放出热量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图Ⅰ是NO2(g)+CO(g) ![]() CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。
CO2(g)+NO(g)反应过程中能量变化的示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ所示。

下列有关说法正确的是
A. 一定条件下,向密闭容器中加入1 mol NO2(g)与1 mol CO(g)反应放出234 kJ热量
B. 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C. 若X表示温度,则Y表示的可能是CO2的物质的量浓度
D. 若X表示反应时间,则Y表示的可能是混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL x mol·L-1 CH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图所示(忽略温度变化)。下列说法中不正确的是( )
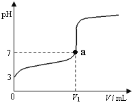
A. 上述 CH3COOH溶液中:c(H+)=1×10-3 mol·L-1
B. 图中V1 <20 mL
C. a点对应的溶液中:c (CH3COO-)=c (Na+)
D. 当加入NaOH溶液的体积为20 mL时,溶液中:c (CH3COOH) + c (H+)>c (OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型锂离子电池的电解质(结构如图,箭头指向表示共同电子对由W原子提供),下列说法还正确的是( )
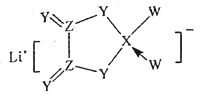
A.气态氢化物的稳定性:W>Y
B.原子半径:X>Z>Y>W
C.该物质中含离子键和共价键
D.Z有多种单质,且硬度都很大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com