
a mol FeS和b mol Fe3O4投入到VL c mol/L的硝酸溶液中恰好完全反应,假设只产生标准状况2.24 L NO气体,溶液中只有Fe(NO3)3和H2SO4的混合液,向溶液中逐渐滴入c′ mol/L NaOH溶液,则当沉淀达最大时,消耗NaOH溶液的体积是
A. L B.
L B. L C.
L C. D .
D . L
L
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 16g氧气 | B. | 0.1mol甲烷分子(CH4) | ||
| C. | 1.8g水 | D. | 含3.01×1022个磷酸分子(H3PO4) |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
常温下,将Cl2缓慢通入水中至饱和,然后再滴加0.1 mol·L-1的NaOH溶液,整个过程中溶液的pH变化曲线如图所示。下列选项正确的是
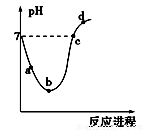
A.a点所示的溶液中[H+]=[Cl-]+[HClO]+[OH-]
B.b点所示的溶液中[H+]>[Cl-]>[HClO]>[ClO-]
C.c点所示的溶液中[Na+]=[HClO]+[ClO-]
D.d点所示的溶液中[Na+]>[ClO-]>[Cl-]>[HClO]
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
全矾液流电池是一种新型电能储存和高效转化装置。某溶液中含有NO3-和Cr2O72-,现向此溶液中滴入29.00mL 0.1mol/L的FeSO4溶液,恰好使VO2+→VO2+、Cr2O72-→Cr3+。再滴入2.00mL 0.020mol/L KMnO4溶液,又恰好使VO2+→VO2+,而Cr3+不变,此时MnO4→Mn2+,则原溶液中Cr的质量为
A. 156 mg B. 234 mg C. 31.2 mg D. 46.8mg
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二次模拟化学试卷(解析版) 题型:填空题
前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻.已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸.
(1)D元素基态原子的电子排布式为____________.
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为_______________(用相应的元素符号作答).
(3)B、X、D氢化物的沸点由高到低的顺序为_______________(用相应的化学式作答).
(4)E元素是A元素所在周期中电负性最大的,试推测下列微粒的立体构型:
微粒 | EO2﹣ | EO3﹣ |
立体构型名称 |
(5)元素B的一种氢化物B2H4具有重要的用途.有关B2H4的说法正确的是____________.
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为____________,δ、γ、α三种晶胞的边长之比为____________。
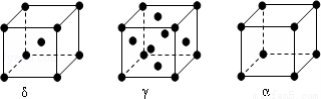
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑦ | B. | ①②⑦ | C. | ②④ | D. | ①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com