
| A. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| B. | 氨气具有还原性,可用作制冷剂 | |
| C. | Na2O2呈浅黄色,可用作潜水艇中的供氧剂 | |
| D. | 氧化铝的熔点高,可用于制造耐火材料 |
分析 A.漂白粉与空气中水、二氧化碳反应生成HClO,具有漂白性;
B.氨气的沸点高,液氨气化时吸热;
C.Na2O2与二氧化碳反应生成氧气;
D.熔点高的物质可作耐火材料.
解答 解:A.漂白粉与空气中水、二氧化碳反应生成HClO,具有漂白性,则漂白粉在空气中不稳定,可用于漂白纸张,故D正确;
B.氨气的沸点高,液氨气化时吸热,则用作制冷剂,与氨气还原性无关,故B错误;
C.Na2O2与二氧化碳反应生成氧气,则用作潜水艇中的供氧剂,与其颜色无关,故C错误;
D.熔点高的物质可作耐火材料,则氧化铝的熔点高,可用于制造耐火材料,故D正确;
故选AD.
点评 本题考查物质的性质及用途,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 食盐水、糖水和冰水都是饮料,属于混合物 | |
| B. | O2不能导电,故O2是非电解质 | |
| C. | 烧碱属于碱,纯碱属于盐 | |
| D. | NaHSO4能电离出氢离子,故NaHSO4属于酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向该容器中充入N2,平衡正向移动 | |
| B. | 降低温度能使混合气体的密度增大 | |
| C. | 该反应达平衡时H2的转化率为20% | |
| D. | 研发高效催化剂可大大提高N2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、NO3-、Cl- | B. | Na+、K+、NO3-、Cl- | ||
| C. | Na+、K+、AlO2-、Cl- | D. | NH4+、K+、SO42-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3被氧化 | B. | NH3是氧化剂 | C. | NO是还原产物 | D. | H2O是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
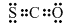 ;生成CO(g)与Sx(s)反应的热化学方程式是xCOS(g)=xCO(g)+Sx(s)△H=0.5x(b-a)kJ/mol
;生成CO(g)与Sx(s)反应的热化学方程式是xCOS(g)=xCO(g)+Sx(s)△H=0.5x(b-a)kJ/mol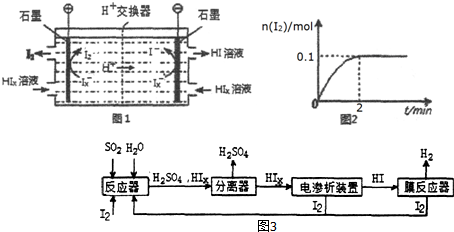
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com