
白磷(P4)分子是正四面体形,4个P原子位于正四面体的四个顶点,如下图所示。
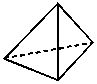
(1)分子中P―P键之间的夹角是_________。
(2)1molP4分子中含有__________molP―P键。
(3)P―P键是__________键(填“非极性”或“极性”)。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2010-2011学年江苏省如皋市五校高二下学期期中调研化学试卷 题型:单选题
下列说法正确的是:

A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱 | B.白磷(P4)分子是正四面体结构,故分子中的键角为1090281 | C.NO2-中心原子采取sp2杂化,分子空间构型为“V”形 | D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
查看答案和解析>>
科目:高中化学 来源:2012届江苏省如皋市五校高二下学期期中调研化学试卷 题型:选择题
下列说法正确的是:
 A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱
A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱
B.白磷(P4)分子是正四面体结构,故分子中的键角为1090281
 C.NO2- 中心原子采取sp2杂化,分子空间构型为“V”形
C.NO2- 中心原子采取sp2杂化,分子空间构型为“V”形
D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
查看答案和解析>>
科目:高中化学 来源:0110 期中题 题型:不定项选择题
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱
B.白磷(P4)分子是正四面体结构,故分子中的键角为1090281
C.NO2- 中心原子采取sp2杂化,分子空间构型为“V”形
D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com