
| A. | Na在空气中久置最终变为NaHCO3粉末 | |
| B. | 向Fe2(SO4)3溶液中加入铜粉,溶液变蓝且有黑色固体析出 | |
| C. | C12能与石灰乳反应,可用于制取漂白粉 | |
| D. | 向KC1O3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
分析 A.NaHCO3粉末在空气中易分解生成碳酸钠;
B.向Fe2(SO4)3溶液中加入铜粉,铜与三价铁反应生成二价铁和二价铜;
C.根据Cl2能与碱反应生成次氯酸盐判断;
D.KC1O3溶液中滴加AgNO3溶液无AgCl沉淀生成.
解答 解:A.NaHCO3粉末在空气中易分解生成碳酸钠,所以Na在空气中久置最终变为碳酸钠,故A错误;
B.向Fe2(SO4)3溶液中加入铜粉,铜与三价铁反应生成二价铁和二价铜,所以溶液变蓝无黑色固体析出,故B错误;
C.工业上用Cl2与石灰乳反应制取漂白粉,故C正确;
D.KC1O3溶液中不含氯离子,所以滴加AgNO3溶液无AgCl沉淀生成,故D错误;
故选C.
点评 本题主要考查了物质的性质与用途,题目较为简单,注意基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
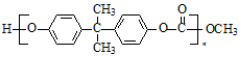

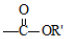 +
+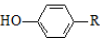 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$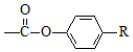 +HOR′
+HOR′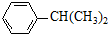 .
.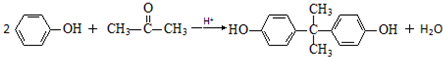 .
.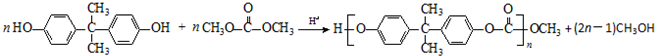 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
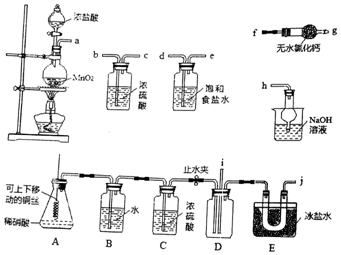
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe( OH)3胶体无色、透明,能发生丁达尔现象 | |
| B. | CO2通入CaCl2溶液中生成CaCO3沉淀 | |
| C. | 将稀硫酸滴加到Fe( NO3)2溶液中无明显现象 | |
| D. | H2、SO2、CO2三种气体都可以用浓硫酸干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
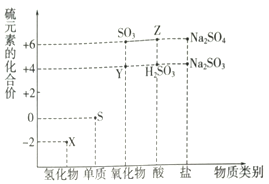 利用元素的化合价推测物质的性质是化学研究的重要手段.
利用元素的化合价推测物质的性质是化学研究的重要手段.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Fe2+、NO3-、Na+、SO42- | |
| B. | c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、Cl-、NO3- | |
| C. | 水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质 | B. | 脂肪 | C. | 多糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com