
【题目】普通水泥在固化过程中自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是( )

A. 工业上以黏土、石灰石和石英为主要原料来制造普通水泥
B. 负极的电极反应式为:2Cu+2OH﹣﹣2e﹣=Cu2O+H2O
C. 测量原理示意图中,电流方向从Cu→Ag2O
D. 电池工作时,OH﹣向正极移动
科目:高中化学 来源: 题型:
【题目】用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素:
Ⅰ.实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理:![]() MnO
MnO![]() +
+![]() H2C2O4+
H2C2O4+![]() ―→
―→![]() Mn2++
Mn2++![]() CO2↑+
CO2↑+![]() H2O
H2O
(1)配平上述离子方程式。______
(2)滴定时KMnO4溶液应盛装于__________(填“酸式”或“碱式”)滴定管中。
Ⅱ.探究影响化学反应速率的因素
实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)探究温度对化学反应速率影响的实验编号是________(填编号,下同)。
(2)探究反应物浓度对化学反应速率影响的实验编号是________。
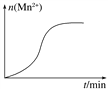
Ⅲ.测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图所示,请解释“n(Mn2+)在反应起始时变化不大,一段时间后快速增大”的原因:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应8NH3+3Cl2==6NH4Cl+N2,回答下列问题:
(1)用单线桥表示出该反应电子转移的数目和方向_____________。
(2)氧化剂是_______。
(3)当有34gNH3参加反应时,被氧化的物质的质量为_____ g,生成的还原产物的质量为_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在光照的条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最多的是( )
A. CH2Cl2 B. CHCl3 C. CCl4 D. HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如下图所示位置,V甲:V乙=4:1(两侧温度、压强均相同)。则混合气体中CO和CO2的物质的量比为( )

A. 1:1 B. 1:3 C. 3:1 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产和生活中有广泛的应用。
(1)铁元素在元素周期表中的位置为________________。
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为__________;铁在高温条件下与水蒸气反应的化学方程式为______________________________________________________________。
(3)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图:

已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe3+ | Fe2+ | Al3+ |
开始沉淀(pH) | 2.3 | 7.5 | 3.4 |
完全沉淀(pH) | 3.2 | 9.7 | 4.4 |
①加入少量NaHCO3的目的是调节pH,应控制pH的范围为____________。
②碱式硫酸铁溶于水后产生的[Fe(OH)]2+,可部分水解生成聚合离子[Fe2(OH)4]2+。该水解反应的离子方程式为_______________________________。
(4)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种。
①熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2===Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4===K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:_________________________________________________________________。
②电解法制备高铁酸钾。铁和石墨分别做两个电极的电极材料,氢氧化钠溶液做电解液实现电解制备。阴极的电极材料为__________,写出阳极的电极反应式为_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于试剂保存正确的是( )
A. 氢氧化钠固体保存在带有橡胶胶塞的细口瓶中
B. 碳酸钠溶液保存在带有橡胶塞的广口瓶中
C. 金属钾保存在煤油中
D. 过氧化钠密封在带玻璃塞的广口瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 2.0gH218O与D2O的混合物中所含中子数为NA
B. 常温常压下4.4g乙醛所含σ键数目为0.7NA
C. 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA
D. 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com