
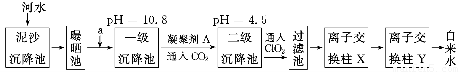
某自来水厂利用河水处理成自来水的工艺流程示意图如下图所示:
提供的试剂:饱和Na2CO3溶液、NaOH溶液、生石灰、CCl4、BaCl2溶液、KOH溶液
(1)为除去水中含有的Ca2+、Mg2+、HCO3-、Cl-、SO42-,试剂a代表两种化学物质,主要是除去水中SO42-、Mg2+和HCO3-,这两种试剂是________和________(只填化学式)。
(2)凝聚剂A常用FeSO4·7H2O,最终生成红褐色胶体沉淀,该胶状沉淀的化学式为________,可以除去其中的悬浮固体颗粒,该过程是________(填序号)。
A.只有物理变化,无化学变化
B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
(3)通入CO2的目的是__________和__________。
(4)传统的氧化剂是Cl2,现代工艺用ClO2取代Cl2,通入ClO2的作用是________________________;优点是________________________________。
(5)离子交换柱X、Y中有一种是H+型交换柱,另一种是OH-型离子交换柱,目的是除去水中残留的杂质离子,则X应是哪种交换柱?________(填“H+型”或“OH-型”);如果两个交换柱位置颠倒会产生什么后果?_______________________________________
________________________________________________________________________。
(1)BaCl2 CaO
(2)Fe(OH)3 C
(3)除去Ca2+ 调节溶液的pH=4.5
(4)杀菌、消毒 高效、强力、无毒、无刺激性气味
(5)H+型 如果先通过OH-型离子交换柱,产生的OH-会与水体中残留的Ca2+、Mg2+等作用生成难溶物而堵塞交换柱
【解析】该工艺流程是自来水的生产过程。(1)除去SO42-用Ba2+,除去Mg2+用OH-,除去HCO3-用OH-和Ca2+,综合所给试剂和要求选用两种试剂,只能选BaCl2和生石灰。(2)氢氧化铁胶体可以吸附水中的悬浮物,使之沉降下来,达到净水的目的,这是物理变化,氢氧化铁胶体是由FeSO4得到的,发生化学变化,选C。(3)由框图流程可知,通入CO2既可以除去Ca2+,又可以降低溶液的pH。(4)Cl2和ClO2都起到杀菌、消毒的作用,ClO2具有高效、强力、无毒、无刺激性气味的优点。(5)应首先经过H+型交换柱,如果先通过OH-型交换柱,产生的OH-会与水体中残留的Ca2+、Mg2+等作用生成难溶物而堵塞交换柱。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:阅读理解
 (2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题:
(2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题:| 物 质 | CO | H2 | CH3OH |
| 浓度/(mol?L-1) | 1.2 | 1.0 | 0.6 |
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
查看答案和解析>>
科目:高中化学 来源:2011届天津市南开区高三一模考试(理综)化学部分 题型:填空题
(14分)能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ · mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ · mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ · mol-1
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。
下列说法中正确的是_____________(填字母序号)。
| A.负极的电极反应式为:CO + O2-―2e-=CO2 |
| B.工作时电子由电极a通过传感器流向电极b |
| C.工作时电极b作正极,O2-由电极a通过固体介质向电极b迁移 |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
 CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:| 物 质 | CO | H2 | CH3OH |
| 浓度/(mol·L-1) | 1.2 | 1.0 | 0.6 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省唐山市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
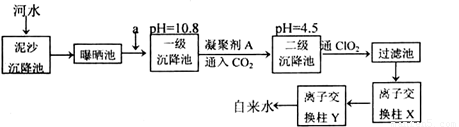
某自来水厂利用河水处理成自来水的工艺流程示意图如下图所示:
提供的试剂:饱和Na2CO3溶液、NaOH溶液、生石灰、CC14、BaCl2溶液,KOH溶液
(1)为除水中含有Ca2+、Mg2+、HCO3-、Cl-、SO42-,试剂a代表两种化学物质,主要是除去水中SO42-、Mg2+和HCO3-,这两种试剂是_______和______(只填化学式)。
(2)凝聚剂A常用FeSO4·7H2O,最终生成红褐色胶状沉淀,该胶状沉淀的化学式为______,可以除去其中的悬浮固体颗粒,该过程是______ (填序号)。
A.只有物理变化,无化学变化 B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
(3)通入CO2的目的是______和______。
(4)传统的氧化剂是Cl2,现代工艺用ClO2取代Cl2,通入CIO2的作用是______,优点是______。
(5)离子交换柱X、Y中有一种是H+型交换柱,另一种是H-型离子交换柱,目的是除去水中残留的杂质离子,则X应是哪种交换柱______(填“H+型”、“OH-型”);如果两个交换柱位置颠倒会产生什么后果____________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年天津市南开区高三一模考试(理综)化学部分 题型:填空题
(14分)能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ · mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ · mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ · mol-1
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。

下列说法中正确的是_____________(填字母序号)。
A.负极的电极反应式为:CO + O2-―2e-=CO2
B.工作时电子由电极a通过传感器流向电极b
C.工作时电极b作正极,O2-由电极a通过固体介质向电极b迁移
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某硝酸厂利用甲醇处理废水。在一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比为______________。
(4)煤的间接液化是先转化为CO和H2,再在催化剂作用下合成甲醇。若在一定温度下,向1 L密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)  CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
|
物 质 |
CO |
H2 |
CH3OH |
|
浓度/(mol·L-1) |
1.2 |
1.0 |
0.6 |
① 该反应的平衡常数表达式为:K=_____________________。
② 该时间内反应速率v(H2)=_________________。
③ 平衡时CO的转化率为_________________(保留1位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com