
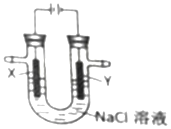
| A. | X电极为阴极 | B. | Y电极为负极 | ||
| C. | X电极表面发生氧化反应 | D. | Y电极表面有氯气生成 |
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:选择题
| A. | 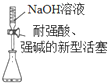 量取10.00mLNaOH溶液 | |
| B. | 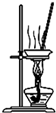 蒸干氯化铜溶液制CuCl2•2H2O | |
| C. | 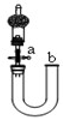 关闭活塞a,从b处加水,以检查装置的气密性 | |
| D. | 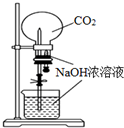 用CO2做喷泉实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气处理饮用水,在冬季的杀菌效果比在夏季好 | |
| B. | 中国古代利用明矾溶液的酸性来清除铜镜表面的铜锈 | |
| C. | 食盐、漂白粉均可以将某些病毒氧化而达到消毒的目的 | |
| D. | 白葡萄酒含维生素C等多种维生素,通常添加微量SO2,以防止营养成分被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁、不锈钢和黄铜都属于合金 | |
| B. | 淀粉、油脂和蛋白质都属于天然高分子化合物 | |
| C. | 水泥、玻璃和陶瓷都属于无机非金属材料 | |
| D. | 天然气、液化石油气和汽油的主要成分都属于烃类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(5)(6) | B. | (3)(4)(5) | C. | (2)(3)(5)(6) | D. | (1)(2)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 该有机物中必定含有碳碳双键 |
| B | 向亚硫酸钠溶液中滴加硝酸钡和稀硝酸 | 产生白色沉淀 | 亚硫酸钠溶液已变质 |
| C | 向酸性高锰酸钾溶液中滴加双氧水 | 紫色褪去,产生气泡 | H2O2具有还原性 |
| D | 向油脂皂化反应后的溶液中滴入酚酞 | 溶液不变红 | 油脂已经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
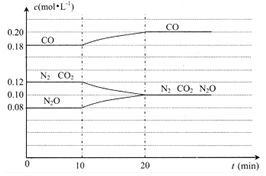 汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.
汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应.| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(N2O) | n(CO) | n(CO2) | ||
| ① | 400 | 0.20 | 0.30 | 0.14 |
| ② | 500 | 0.10 | 0.40 | 0.080 |
| ③ | 500 | 0.30 | 0.20 | A |
| ④ | 600 | 0.60 | 0.40 | B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的NaN3和Na2O2中所含阴离子数均为NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA | |
| C. | 标准状况下,将3.36LCl2通入1L 0.2mol•L-1FeBr2溶液中,被氧化的Br-数目为0.1NA | |
| D. | 标准状况下,11g由${\;}_{1}^{3}$H和${\;}_{8}^{16}$O组成的超重水中,中子数和电子数之和为10NA |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一上第一次月考化学试卷(解析版) 题型:实验题
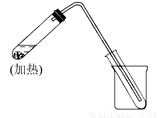
(1)左边大试管中要加入几片碎瓷片,其作用是_______________________;
(2)该装置中使用的玻璃导管较长,其作用是_________________________;
(3)烧杯中还要盛有的物质是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com