
| A. | 过氧化钠的电子式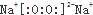 | B. | CO2的电子式: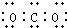 | ||
| C. | 12753I和12953I2互为同位素 | D. | 硫离子的结构示意图: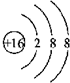 |
分析 A.过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物;
B.二氧化碳分子中存在两个碳氧双键;
C.同位素为质子数相同,中子数不同的原子;
D.硫离子的核电荷数为16,核外电子总数为18.
解答 解:A.过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为: ,故A错误;
,故A错误;
B.二氧化碳为共价化合物,分子中存在两个碳氧双键,不存在碳氧单键,二氧化碳正确的电子式为: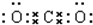 ,故B错误;
,故B错误;
C.同位素为质子数相同,中子数不同的原子,而12953I2为单质,故C错误;
D.硫离子的核外电子总数为18,最外层为8个电子,硫离子的结构示意图为: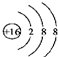 ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、原子结构示意图与离子结构示意图、同位素等化学用语的概念及书写原则.


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:选择题
| A. | C12 | B. | NH3 | C. | BaCO3 | D. | C2H5OH (乙醇) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1L0.1mol/L的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 1mol羟基中电子数为10NA | |
| C. | 在含4mol Si-O键的二氧化硅中,氧原子数为4NA | |
| D. | 常温常压下,22.4L乙烯中C-H键数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
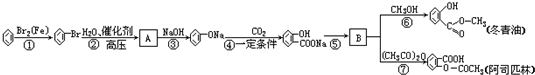
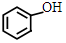 ;
; .
.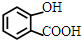 +NaHCO3→
+NaHCO3→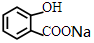 +CO2↑+H2O.
+CO2↑+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
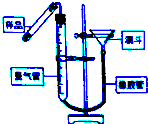 过氧化钙(CaO2•8H2O)是一种在水产养殖中广泛使用的供氧剂.
过氧化钙(CaO2•8H2O)是一种在水产养殖中广泛使用的供氧剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氧化剂只有FeCl3 | |
| B. | NaBH4的电子式为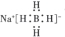 | |
| C. | NaBH4与稀硫酸不发生反应 | |
| D. | 该反应中每生成1 mol Fe,转移的电子数为3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
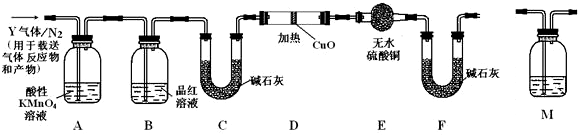
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com