
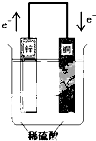
| A、铜片上有大量气泡产生 |
| B、铜片上发生氧化反应 |
| C、锌片为负极 |
| D、该装置将化学能转化为电能 |
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
| +X,一定条件 |
| 反应① |
| +X,一定条件 |
| 反应② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、分子式是C13H14O4Cl2 |
| B、1mol利尿酸最多能与5mol H2发生加成反应 |
| C、-定条件下能发生加聚、缩聚反应 |
| D、分子中所有碳原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Fe作负极,发生氧化反应 |
| B、盐桥的作用是平衡电荷,构成闭合回路 |
| C、工作一段时间后,NaCl溶液中c(Cl-)不变 |
| D、正极反应:2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Mg2+、Cl-、NO3- |
| B、Ba2+、SO42-、Cl-、OH- |
| C、K+、OH-、CO32-、MnO4- |
| D、Ca2+、K+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③④ |
| C、②⑤⑥ | D、⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com