
| A. | 2L溶液中阴、阳离子总数为1.2NA | |
| B. | 100mL溶液中NO3-物质的量为为0.4mol | |
| C. | 200mL溶液中Mg2+浓度为0.2mol•L-1 | |
| D. | 500mL溶液中NO3-总数为0.2NA |
分析 A.求出Mg(NO3)2的物质的量,而1molMg(NO3)2中含3mol离子;
B.0.2mol•L-1的Mg(NO3)2溶液,硝酸根离子浓度为0.4mol/L;
C.0.2mol•L-1的Mg(NO3)2溶液,硝酸根离子浓度为0.2mol/L,溶液浓度与溶液体积无关;
D.0.2mol•L-1的Mg(NO3)2溶液,硝酸根离子浓度为0.4mol/L,依据N=CVNA计算.
解答 解:A.1molMg(NO3)2中含3mol离子,1L 0.2mol•L-1的Mg(NO3)2溶液含有硝酸镁的物质的量为1L×0.2mol/L=0.2mol,则2L溶液中含有硝酸镁为0.2mol×2=0.4mol,含有阴、阳离子总数为1.2NA,故A正确;
B.0.2mol•L-1的Mg(NO3)2溶液,硝酸根离子浓度为0.4mol/L,100mL溶液中NO3-物质的量为0.4mol×0.1L=0.04mol,故B错误;
C.0.2mol•L-1的Mg(NO3)2溶液,硝酸根离子浓度为0.2mol/L,故C正确;
D.500mL溶液中NO3-总数为0.4mol/L×0.5L×NA=0.2NA,故D正确;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意溶质与离子之间浓度大小关系.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 20℃ | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |
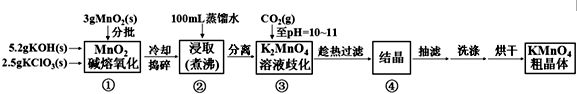
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | NO3-、K+、Cl-、Na+ | D. | K+、Cl-、Al3+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
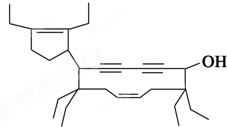 有一种有机物的键线式酷似牛(如图),故称牛式二烯炔醇.下列有关说法不正确的是(已知1mol-C≡C-与H2反应时相当于2mol
有一种有机物的键线式酷似牛(如图),故称牛式二烯炔醇.下列有关说法不正确的是(已知1mol-C≡C-与H2反应时相当于2mol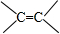 )( )
)( )| A. | 牛式二烯炔醇在水中的溶解度比乙醇小 | |
| B. | 牛式二烯炔醇分子能被催化氧化 | |
| C. | 1mol牛式二烯炔醇最多可与6molH2发生加成反应 | |
| D. | 牛式二烯炔醇的分子式为C29H43O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 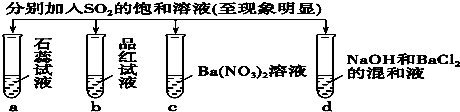 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应的本质是有化合价的升降 | |
| B. | 据丁达尔效应可将分散系分为溶液、胶体与浊液 | |
| C. | 向醋酸溶液中加入少量氢氧化钠溶液,由于发生中和反应,溶液的导电能力降低 | |
| D. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第二位 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com