
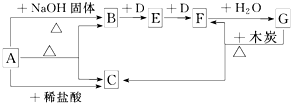
分析 B是能使湿润的红色石蕊试纸变蓝色的无色气体是NH3,是A和氢氧化钠反应生成,说明A中含铵根离子,B和D发生两部连续反应,说明D是无色无味的气体O2,E为NO,F为NO2,G为HNO3,G和C反应生成二氧化氮和二氧化碳,所以C为CO2,A是一种酸式盐,确定A为碳酸氢铵;依据判断出的物质分析回答.
解答 解:A是一种酸式盐,也是一种常用的化学肥料,B是能使湿润的红色石蕊试纸变蓝色的无色气体是NH3,是A和氢氧化钠反应生成,说明A中含铵根离子,B和D发生两部连续反应,说明D是无色无味的气体O2,E为NO,F为NO2,G为HNO3,G和C反应生成二氧化氮和二氧化碳,所以C为CO2,A是一种酸式盐,确定A为碳酸氢铵,
(1)根据上面的分析可知,A为碳酸氢铵,
故答案为:碳酸氢铵;
(2)物质B是NH3,工业用途可以工业制硝酸(或制氮肥,制氨水等),
故答案为:工业制硝酸(或制氮肥,制氨水等);
(3)B是NH3,实验室制取气体B的化学方程式为2NH4Cl+Ca(0H)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,工业上制取气体B是用氢气和氮气高温高压催化剂条件下合成氨,反应的化学方程式为:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,
故答案为:2NH4Cl+Ca(0H)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;
(4)B-→E反应的化学方程式为4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O,F→G反应的化学方程式为3NO2+H2O=2HNO3+NO,
故答案为:4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O;3NO2+H2O=2HNO3+NO.
点评 本题考查了无机物质转化关系的推断,物质性质的应用,主要考查氮及其化合物性质的应用,碳酸盐的性质应用,工业制备氨气、硝酸等物质的原理应用,关键是B和D发生两部连续反应,说明D是无色无味的气体O2的判断.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
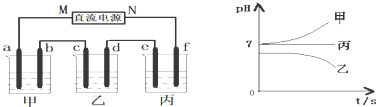
 根据实验装置和下述操作,回答下列有关问题:
根据实验装置和下述操作,回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种金属物质的量相等 | B. | 三种金属均过量 | ||
| C. | 三种金属的质量相等 | D. | 盐酸均过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结构简式为 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 | |
| B. | 分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 | |
| C. | 某有机物球棍结构模型为: ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 | |
| D. | 二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com