
| A、21.2g |
| B、21.6g |
| C、22.0g |
| D、22.4g |
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
| A、用洁净的玻璃棒蘸取试液,点在湿润的pH 试纸上测定试液pH |
| B、在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液 |
| C、用25mL 酸式滴定管量取18.00mL KMnO4溶液 |
| D、为减小中和滴定误差,锥形瓶必须洗净烘干并用待测液润洗后才能使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
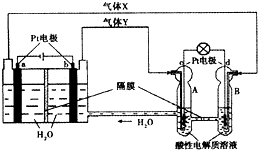 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A、当有0.2mol电子转移时,a极产生1.12L O2 |
| B、该装置开始工作后,右端装置能量变化为:电能→化学能 |
| C、d极上发生的电极反应是:O2+4H++4e一═2H2O |
| D、c极上进行还原反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子间的相互作用叫做化学键 |
| B、第三周期元素的最高正化合价等于它所处的主族序数 |
| C、VIIA 族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强 |
| D、元素种类由质子数决定,元素原子的化学性质由最外层电子数决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、溶质的物质的量浓度c=
| ||
B、溶质的质量分数为ω=
| ||
C、溶液中c(OH-)=
| ||
| D、上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5molNaCl溶解在1 L水中,所得溶液的物质的量浓度为0.5 mol/L |
| B、10mL 1 mol/L的H2SO4溶液与100mL 1 mol/L的K2SO4溶液中,SO42-的物质的量浓度相同 |
| C、标准状况下,22.4L水的质量为18g |
| D、常温常压下,1molCH4的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL3mol/LKClO3溶液 |
| B、75mL2.5mol/LMgCl2溶液 |
| C、150mL3mol/LKCl溶液 |
| D、25mL2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com