

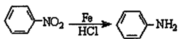
 ,-NH2易被强氧化剂氧化
,-NH2易被强氧化剂氧化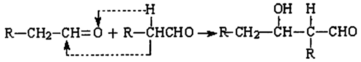
 .
. .
. .
. .
.分析 由甲苯与氯气在光照条件下发生的取代反应得到A为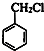 ,A与NaOH溶液发生水解反应生成B为
,A与NaOH溶液发生水解反应生成B为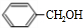 ,B再发生催化氧化生成C为
,B再发生催化氧化生成C为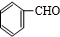 ,由信息(2)可知,苯甲醛与乙醛在碱性条件下得到D为
,由信息(2)可知,苯甲醛与乙醛在碱性条件下得到D为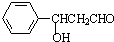 ,则试剂X为CH3CHO,D再发生消去反应得到E为
,则试剂X为CH3CHO,D再发生消去反应得到E为 ,
, 发生银镜反应后再酸化得到F为
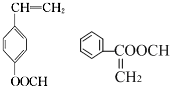
发生银镜反应后再酸化得到F为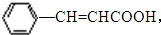 ,F与甲醇发生酯化反应生成肉桂酸甲酯P为
,F与甲醇发生酯化反应生成肉桂酸甲酯P为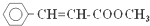 ;
;
由甲苯与G的分子式,结合N的结构简式可知,甲苯发生甲基对位的硝化反应生成G,则G为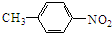 ,G发生信息(1)反应,硝基被还原为氨基生成H,则H的结构简式为
,G发生信息(1)反应,硝基被还原为氨基生成H,则H的结构简式为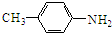 ,结合N的结构可知,H中氨基中1个H原子被取代生成M为
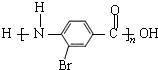
,结合N的结构可知,H中氨基中1个H原子被取代生成M为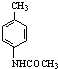 ,M被酸性高锰酸钾溶液氧化生成N,对比N、Q的结构可知,N与液溴发生取代反应生成W,W发生水解反应得到Q,结合题目分析解答.
,M被酸性高锰酸钾溶液氧化生成N,对比N、Q的结构可知,N与液溴发生取代反应生成W,W发生水解反应得到Q,结合题目分析解答.
解答 解:(1)根据以上分析,肉桂酸甲酯P为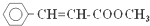 ,则分子中官能团的名称是酯基和碳碳双键,试剂X的结构简式CH3CHO,D发生消去反应得到E,故答案为:酯基和碳碳双键;CH3CHO;消去反应;
,则分子中官能团的名称是酯基和碳碳双键,试剂X的结构简式CH3CHO,D发生消去反应得到E,故答案为:酯基和碳碳双键;CH3CHO;消去反应;
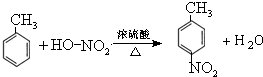
(2)①甲苯发生甲基对位的硝化反应生成G,则甲苯→G的方程式为: ,
,
故答案为: ;
;
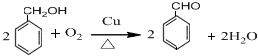
②B再发生催化氧化生成C,则B→C的方程式为: ,
,
故答案为: ;
;
(3)因为氨基易被氧化,故在苯环上的甲基被氧化成羧基反应之前需先保护氨基,所以在合成Q的过程中,H→M步骤不能省略;Q中的羧基和氨基能脱水生成形成高分子化合物,则Q在一定条件下形成高分子化合物的结构简式为 ,
,
故答案为:因为氨基易被氧化,故在苯环上的甲基被氧化成羧基反应之前需先保护氨基; ;
;
(4)E为 ,含有碳碳双键和醛基,所以检验E分子中含有碳碳双键,应先用银氨溶液(或新制的氢氧化铜悬浊液)将醛基氧化,后用溴水检验碳碳双键,所以所需要的试剂为银氨溶液(或新制的氢氧化铜悬浊液),溴水,
,含有碳碳双键和醛基,所以检验E分子中含有碳碳双键,应先用银氨溶液(或新制的氢氧化铜悬浊液)将醛基氧化,后用溴水检验碳碳双键,所以所需要的试剂为银氨溶液(或新制的氢氧化铜悬浊液),溴水,
故答案为:银氨溶液(或新制的氢氧化铜悬浊液),溴水;
(5)F为C6H5-CH=CHCOOH,①能发生水解反应②与银氨溶液作用出现光亮的银镜,则含有酯基又含有醛基,又只含2个O,所以为甲酸酯;③能与溴发生加成反应,说明含有碳碳双键,所以符合条件的同分异构体为C6H5-CH=CH-OOCH、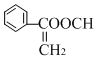 两种,苯环有2个取代基的为-CH=CH2和-OOCH,有邻间对3种,所以符合条件的同分异构体共有5种,其中分子核磁共振氢谱有5种峰的物质结构简式为
两种,苯环有2个取代基的为-CH=CH2和-OOCH,有邻间对3种,所以符合条件的同分异构体共有5种,其中分子核磁共振氢谱有5种峰的物质结构简式为 ,
,
故答案为:5; .
.
点评 本题考查有机推断,为高考高频点,侧重考查学生分析推断、知识迁移及知识综合应用能力,根据流程图中物质结构变化及反应条件进行推断,熟悉常见有机反应类型及反应条件,题目难度中等.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:选择题
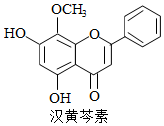 汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用.下列有关汉黄芩素的叙述正确的是( )
汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用.下列有关汉黄芩素的叙述正确的是( )| A. | 汉黄芩素的分子式为C16H13O5 | |
| B. | 该物质遇FeCl3溶液显色 | |
| C. | 1 mol该物质与溴水反应,最多消耗1mol Br2 | |
| D. | 与足量H2发生加成反应后,该分子中官能团的种类减少1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:NH3>H2O>HF | B. | 离子半径:Na+<Mg2+<Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H2CO3 | D. | 金属还原性:Mg>Ca |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水显酸性的主要原因:HClO?H++ClO- | |
| B. | 向氯水中滴加少量NaHCO3溶液:H++HCO3-═CO2↑+H2O | |
| C. | SO2具有漂白性,向氯水中通入少量SO2,溶液的漂白能力降低 | |
| D. | 常温时,氯水中含有的阴离子:Cl-、ClO-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.  .
. $→_{K_{2}CO_{3}}^{(CH_{3})_{2}SO_{4}}$
$→_{K_{2}CO_{3}}^{(CH_{3})_{2}SO_{4}}$ (R代表烃基,R'代表烃基或H) 请写出以
(R代表烃基,R'代表烃基或H) 请写出以 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
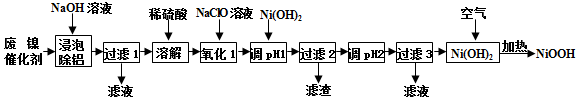
| 开始沉淀的pH | 完全沉淀的pH | |
| Ni2+ | 6.2 | 8.6 |
| Fe2+ | 7.6 | 9.1 |
| Fe3+ | 2.3 | 3.3 |
| Cr3+ | 4.5 | 5.6 |
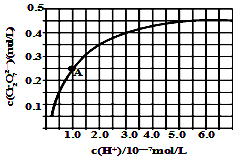
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤干馏后得到的焦炉煤气主要含有甲烷、氢气、乙烯和一氧化碳等 | |
| B. | 生活中常见的有机玻璃的主要成分是聚甲基丙烯酸甲酯,它是一种有机聚合物 | |
| C. | 阿斯匹林、去痛片等药片是用淀粉作为粘合材料压制而成的片剂 | |
| D. | 成熟苹果的汁液能与银氨溶液发生反应,是因为苹果中含有大量的淀粉和纤维素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
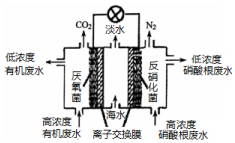
| A. | 该电池能在高温下工作 | |
| B. | 该电池工作时,中间室中的Cl-移向右室 | |
| C. | 正极上发生的电极反应:2NO3-+6H2O+10e-═N2↑+12OH- | |
| D. | 若有机废水中有机物用C6H12O6表示,每消耗1 mol C6H12O6转移4 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com