
铁黄是一种重要的颜料,化学式为Fe2O3·xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如下:
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是 、 。
(2)试剂a最好选用 (供选择使用的有:铝粉、空气、浓HNO3);其作用是 。
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是 (填序号)。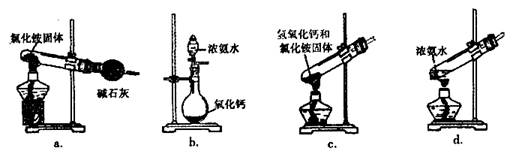
(4)检验溶液Z中含有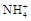 的方法是 。
的方法是 。
(5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。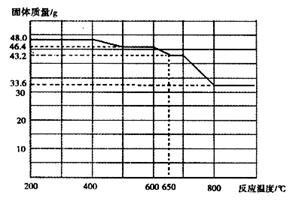
根据图象推断670℃时Fe2O3还原产物的化学式为 ,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论)。 。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。
(11分)(1)搅拌加速溶解(或搅拌加速反应)(1分)(只答搅拌也得分) 引流(1分)
(2)空气(1分) 作氧化剂,将Fe2+氧化为Fe3+(1分)(答氧化剂、氧化Fe2+或将Fe2+转化为Fe3+也得分)
(3)bd(2分)
(4)取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+。(2分)(三个要点:浓NaOH溶液、湿润的红色石蕊试纸、变蓝。缺一个要点扣1分)
(5)FeO(1分)取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO。(2分)(要点:三组操作与现象、最终结论,少一个扣1分)
解析试题分析:(1)操作Ⅰ是物质的溶解,操作Ⅱ是过滤,都需要用到玻璃棒,玻璃棒在两种操作中的作用分别是,操作Ⅰ是利用玻璃棒加速硫酸渣的溶解,操作Ⅱ中玻璃棒是起到引流作用。
(2)依据流程分析,溶液Y中含有亚铁离子,需要将其氧化成铁离子,因此试剂a主要是用来氧化亚铁离子的。但选择氧化剂不能引入新的杂质,铝粉引入新的杂质,浓硝酸做氧化剂会产生污染气体,最好选择空气做氧化剂氧化亚铁离子,不会引入新的杂质,不污染环境。
(3)a、加热氯化铵分解后生成氨气和氯化氢会在试管口重新生成氯化铵;不能制的氨气,故a不能;
b、氨水滴入氧化钙固体,氧化钙会和水反应生成氢氧化钙放热,使一水合氨分解生成氨气;故b符合;
c、氢氧化钙和氯化铵固体加热时需要试管口略向下倾斜,装置中加热会使生成的水倒流到试管底部炸裂试管;故c不选;
d、加热浓氨水会分解生成氨气,可以制取氨气;故d符合,因此答案为bd。
(4)NH4+能和强碱反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝,通过检验氨气的方法来检验NH4+,所以检验溶液Z中含NH4+的实验方法是:取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+。
(5)根据图像可知,加热前氧化铁的物质的量是48g÷160g/mol=0.3mol。加热到670℃时固体质量变为43.2g,即固体质量减少48g-43.2g=4.8g,减少的质量即为氧原子的质量,所以减少的氧原子质量是4.8g÷16g/mol=0.3mol,则根据原子守恒可知,反应后铁原子和氧原子的个数之比是(0.3mol×2):(0.3mol×3-0.3mol)=1:1,所以该固体的化学式是FeO。要检验还原产物,可以通过检验亚铁离子和铁离子的方法来验证,另外还需要排除单质铁,所以正确的操作是取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO。
考点:考查玻璃棒的作用、试剂的选择、氨气的制备和NH4+的检验、氧化铁与CO反应生成物的判断和计算、亚铁离子和铁离子的检验等


科目:高中化学 来源: 题型:实验题
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。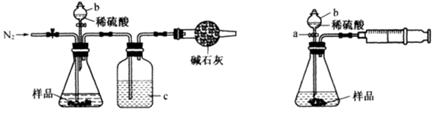
图1 图2
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的 (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是 。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3”质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的 上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的 (填“体积’’或“质量’’)。
(3)丙同学用下图所示方法和步骤实验: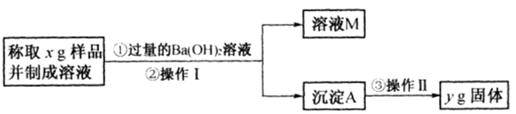
①操作I涉及的实验名称有 、洗涤;操作Ⅱ涉及的实验名称有干燥、 。
②丙测得的样品中Na2CO3质量分数的计算式为 。
(4)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计) 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为测定某补血剂样品〔主要成分是硫酸亚铁晶体(FeSO4·7H2O)〕中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
⑴写出滴定反应的离子方程式 。
(2)下列滴定方式中,最合理的是 (夹持仪器略去)(填字母序号〕
(3)实验前,首先要准确配制一定物质的量浓度的酸性KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需_ (填仪器名称)。
(4)若某同学取5片补血剂样品配成100 mL溶液,取20. 00 mL试样,用浓度为c1mol·L-1的KMnO4溶液滴定,耗去V1 mL,则每片补血剂含铁元素的质量_ g(用代数式表示)。
方案二:将FeSO4转化为Fe2O3,测定质量变化。操作流程如下: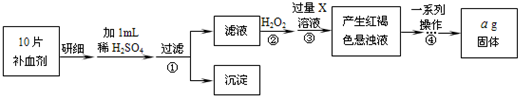
(5)步骤②中用H2O2的目的是_ _。
(6)步骤④中一系列操作依次是:过滤、洗涤、_ 、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量为_ g(用含a的代数式表示)。
(8)若某同学设计以原电池的形式实现Fe2+至Fe3+的转化,正极通人O2,电解质溶液为稀硫酸,请写出正极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
【查阅资料】2KNO3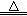 2KNO2+O2↑ Fe(NO3)2
2KNO2+O2↑ Fe(NO3)2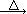 FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)【提纯猜想】
猜想一:铁元素只显+2价;
猜想二:铁元素 ;
猜想三:铁元素既有+2价又有+3价。
【实验操作】①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)【实验现象】实验① ;实验② 。
(3)【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是 。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量Fe(NO3)2固体于试管中,加热分解。 | ,说明分解产生的气体中含有NO2。 |
| 步骤2:将产生的气体依次通过盛有足量 、浓硫酸的洗气瓶, 在最后一个出口检验。 | ,说明分解产生的气体中含O2。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。有研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。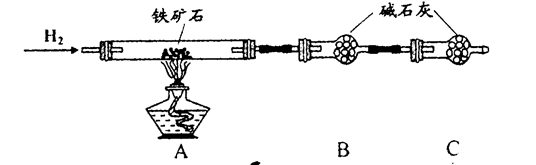
实验一:铁矿石中含氧量的测定
a.按上图组装仪器(夹持仪器均省略),检查装置的气密性;
b.将5.0g铁矿石放入硬质玻璃管中;
c.从左端导气管口处不断地缓缓通入H2,待C装置出口处对H2验纯后,点燃A处酒精灯;
d.充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为_______________________________________________________。
(2)测得反应后装置B增重1.35g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定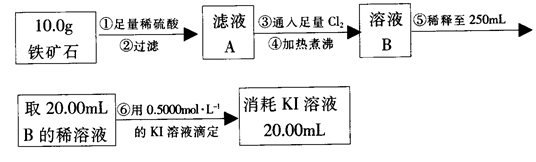
(3)步骤④中煮沸的目的是_____________________________________________。
(4)步骤⑤中用到的玻璃仪器有烧杯、胶头滴管、_________________________。
(5)下列有关步骤⑥的操作中说法不正确的是_______________________________。
a.滴定管用蒸馏水洗涤后再用待装液润洗
b.锥形瓶不需要用待测液润洗
c.因为碘水为黄色,所以滴定过程中不需加指示剂
d.滴定过程中可利用淀粉溶液作为指示剂
(6)铁矿石中铁的质量分数为______________________________________________。
实验结论:推算铁的氧化物的组成
(7)由实验一、二得出该铁矿石中铁的氧化物的化学式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列装置测定铁触媒的含铁量,确定其组成。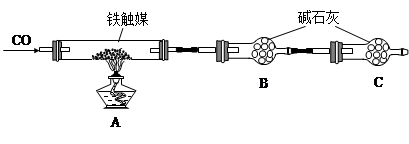
方案二:用下列实验方法测定铁触媒的含铁量,确定其组成。
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
(2)因为通入Cl2不足量,“溶液B”中还含有 会影响测定结果。
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液
| 实验操作 | 实验现象与结论 |
| | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL的浓硝酸恰好完全反应,产生气体4.48 L(标准状况),则下列说法正确的是
| A.产生的气体是0.2 mol NO2 |
| B.硝酸的物质的量浓度为12 mol·L-1 |
| C.反应中被还原和未被还原的硝酸物质的量之比为3∶2 |
| D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
把3体积的NO2气体,依次通过下列3个分别装有①NaHCO3饱和溶液②浓H2SO4③Na2O2的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是(同温同压下测定)
| A.1体积NO | B.2体积NO2和0.5体积O2 |
| C.2体积O2 | D.0.25体积O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com