
【题目】自来水生产过程中,可用氯气等物质作消毒剂,明矾等物质作絮凝剂。出厂的自来水中含少量可溶性矿物质。完成下列填空:
(1)自来水中含硫量约70 mg/L,它只能以______(填微粒符号)形态存在,不能以其它形态存在的原因是________________________。
(2)已知在碱性条件下,氯气会发生自身氧化还原反应,某反应体系中的物质为:KClO3、Cl2、KCl、KOH、H2O。
①写出该反应的化学方程式。____________________________。
②该反应中氧化剂与还原剂的质量比为_________。
(3)实验室利用反应6HCl+KClO3 → KCl+3H2O+3Cl2↑制取Cl2,当产生标准状况下的气体3.36 L时,转移电子_____mol。
(4)不同环境中,物质的性质可能会有所不同。根据上述两题的反应中KClO3和Cl2的氧化性强弱比较,你能得出的结论是________________________。
(5)铝铵矾[NH4Al(SO4)212H2O]也是常用的工业净水剂,其净水的化学原理是________________(用离子方程式表示)。
(6)在向铝铵矾溶液中逐滴滴加氢氧化钡溶液的过程中,下列关系可能正确的是_________。(选填编号)
a.n(SO42-)>n(NH4+)>n(A13+)>n(OH-)
b.n(A13+)>n(NH4+)>n(SO42-)>n(H+)
c.n(BaSO4)>n[A1(OH)3]>n(NH3·H2O)>n(A1O2-)
d.n(NH3·H2O)>n(BaSO4)>n[A1(OH)3]>n(A1O2-)
【答案】SO42- 自来水中有Cl2,具有强氧化性。(或者SO42-是硫最稳定的化合态) 3Cl2+6KOH=5KCl+KClO3+3H2O 5:1 0.25 酸碱性不同,氯气和氯酸钾的氧化性强弱不同(或碱性条件下,氯气氧化性强;酸性条件下,氯酸钾氧化性强) Al3++3H2O![]() Al(OH)3+3H+ ac
Al(OH)3+3H+ ac
【解析】
(1)自来水中含有氯气,氯气具有强氧化性,能把含S化合物转化为硫酸根离子;
(2)①氯气与KOH反应生成KClO3、KCl和H2O,根据电子守恒、原子守恒,可得反应方程式;
②氧化剂得电子,还原剂失电子,根据得失电子守恒分析;
(3)根据方程式中转移电子数目与反应产生氯气的物质的量关系进行计算;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中,生成3 mol Cl2转移5 mol电子;
(4)物质的氧化性强弱与溶液的酸碱性有关;
(5)铝离子水解生成氢氧化铝胶体能净水;
(6)a.向硫酸铝铵矾溶液NH4Al(SO4)2中滴加极少量的氢氧化钡溶液,溶液相当于铝铵矾溶液;
b.滴加氢氧化钡溶液首先与铝离子反应,所以整个过程中n(Al3+)<n(NH4+);
c.当硫酸根离子完全沉淀,则铵根离子部分反应,则铝离子全部变成氢氧化铝,而偏铝酸根离子的物质的量为0,由此分析解答;
d.溶液中硫酸钡的物质的量最大,所以不可能出现n(NH3H2O)>n(BaSO4)。
(1)自来水中含有氯气,氯气具有强氧化性,能把含S化合物转化为硫酸根离子,所以自来水中的硫以SO42-的形态存在;
(2)①氯气与KOH反应生成KClO3、KCl和H2O,其反应的化学方程式为:3Cl2+6KOH=5KCl+KClO3+3H2O;
②在该反应中,Cl2作氧化剂得电子,Cl2作还原剂失电子,在方程式3Cl2+6KOH=5KCl+KClO3+3H2O中,3 mol Cl2中含有6 mol Cl原子,其中得电子的Cl为5,失电子的Cl为1,则氧化剂与还原剂的物质的量之比为5:1;
(3)在反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中,生成3 mol Cl2转移5 mol电子,制取标准状况下3.36 L氯气的物质的量n(Cl2)=![]() =
=![]() =0.15 mol,则转移电子的物质的量为n(e-)=0.15 mol×
=0.15 mol,则转移电子的物质的量为n(e-)=0.15 mol×![]() =0.25 mol;
=0.25 mol;
(4)酸性条件下发生氧化还原反应,KClO3作氧化剂,碱性条件下,氯气是氧化剂,则溶液的酸碱性不同,氯气和氯酸钾的氧化性强弱不同;
(5)铝铵矾[NH4Al(SO4)212H2O]是常用的工业净水剂,在水中电离出Al3+,Al3+水解生成Al(OH)3胶体表面积大,吸附力强,能够吸附水中悬浮的固体颗粒使之形成沉淀,从而具有净水作用,其水解的离子方程式为:Al3++3H2O![]() Al(OH)3(胶体)+3H+;
Al(OH)3(胶体)+3H+;
(6)a.向硫酸铝铵矾溶液NH4Al(SO4)2中滴加极少量的氢氧化钡溶液,相当于铝铵矾溶液,所以离子浓度为:n(SO42-)>n(NH4+)>n(Al3+)>n(H+)>n(OH-),a正确;
b.滴加氢氧化钡溶液首先与Al3+反应,所以整个过程中n(Al3+)<n(NH4+),b错误;
c.当SO42-完全沉淀,NH4+部分反应,则Al3+全部变成Al(OH)3,而AlO2-的物质的量为0,所以离子物质的量大小关系为:n(BaSO4)>n[A1(OH)3]>n(NH3·H2O)>n(A1O2-),c正确;
d.NH4Al(SO4)2中,SO42-的物质的量是NH4+的2倍,则溶液中BaSO4的物质的量最大,所以不可能出现n(NH3·H2O)> n(BaSO4),d错误;
故合理选项是ac。/p>


科目:高中化学 来源: 题型:
【题目】在同温同压下,分别用如图所示的气体吹出体积相等的甲、乙两个气球,则这两个气球中气体的有关量之比(甲:乙)正确的是

A.质量之比为![]() B.原子总数之比为
B.原子总数之比为![]()
C.分子总数之比为![]() D.碳原子数之比为
D.碳原子数之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,关于a g亚硫酸钠晶体(Na2SO37H2O)的说法中正确的是
A.含Na+数目为![]() NAB.含氧原子数目为
NAB.含氧原子数目为![]() NA
NA
C.完全氧化SO32-时转移电子数目为![]() NAD.含结晶水分子数目为
NAD.含结晶水分子数目为![]() NA
NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)。

①实验1、2研究的是__________对H2O2分解速率的影响。
②实验2、3的目的是_______________对H2O2分解速率的影响。
(2)查文献可知,Cu2+对H2O2分解也有催化作用,为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

①定性如图甲可通过观察_______,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是_________。
②定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是__________。
(3)酸性高锰酸钾溶液和草酸溶液可发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,实验时发现开始反应速率较慢,溶液褪色不明显,但一段时间后突然褪色,反应速率明显加快。对此展开讨论:
①某同学认为KMnO4与H2C2O4的反应是______热反应,导致_______________;
②从影响化学反应速率的因素看,你认为还可能是________的影响。要证明你的猜想,实验方案是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(molL﹣1s﹣1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示的关系:υ(B)=3υ(A); 3υ(C)=2υ(B)。则此反应可表示为( )
A. 2A+3B![]() 2CB. A+3B
2CB. A+3B![]() 2C
2C
C. 3A+B![]() 2CD. A+B
2CD. A+B![]() C
C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.硝酸钾用途广泛,工业上一般用复分解反应制取硝酸钾(相关物质的溶解度曲线见表)。以硝酸钠和氯化钾为原料制备硝酸钾的工艺流程如下:
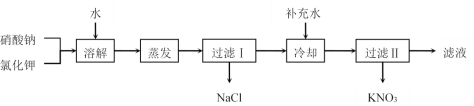
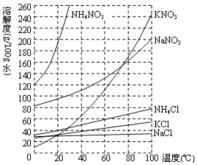
完成下列填空:
(1)为了加速固体溶解,可采取的措施有__________(至少写两种);实验室进行蒸发结晶操作时,为了防止液滴飞溅,进行的操作是_____________。
(2)过滤I所得滤液中含有的离子是________;过滤I所得滤液在进行冷却结晶前应补充少量水,目的是______________。
(3)检验产品KNO3中杂质的方法是________________。
II.实验室模拟工业上用氯化钾和硝酸铵为原料制取硝酸钾的过程如下:
取40 g NH4NO3和37.25 g KCl固体加入100 g水中,加热至90℃,固体溶解, 用冰水浴冷却至5℃以下,过滤(a)。在滤液中再加入NH4NO3,加热蒸发,当体积减小到约原来的![]() 时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
时,保持70℃过滤(b),滤液可循环使用。完成下列填空:
(4)过滤(a)得到的固体物质主要是__________;在滤液中再加入NH4NO3的目的是________________________。
(5)为检测硝酸钾样品中铵盐含量,称取1.564 g样品,加入足量的NaOH浓溶液,充分加热,生成的气体用20.00 mL 0.102 mol/L H2SO4溶液全部吸收,滴定过量的H2SO4用去0.089 mol/L标准NaOH溶液16.55 mL。滴定过程中使用的指示剂是________;样品中含铵盐(以氯化铵计)的质量分数是___________(保留3位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式: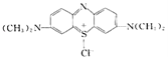
著名的蓝瓶子实验操作步骤如下:
①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:
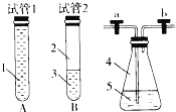
(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________(填“A”或“B”);
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________(填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________(填“能”或“不能”);
(3)上述转化过程中,葡萄糖的作用是_________,亚甲基蓝的作用是_________;
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____;
(5)该实验中③、④操作能否无限次重复进行_________(填“能”或“不能”),理由是 _____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知重铬酸钾(K2Cr2O7)具有强氧化性,其还原产物Cr3+在水溶液中呈绿色或蓝绿色。在K2Cr2O7溶液中存在下列平衡:Cr2O72- (橙色)+H2O![]() 2CrO42- (黄色)+2H+。用K2Cr2O7溶液进行实验,结合实验,下列说法正确的是
2CrO42- (黄色)+2H+。用K2Cr2O7溶液进行实验,结合实验,下列说法正确的是
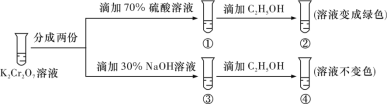
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH氧化
C.对比②和④可知K2Cr2O7碱性溶液氧化性强
D.若向④中加入70% H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下2L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
X | Y | W | |
n(起始状态)/mol | 2 | 1 | 0 |
n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下达平衡后,增大压强平衡不移动
B.该反应方程式可表示为:X+2Y=3W
C.升高温度,若W的体积分数减小,则此反应ΔH>0
D.恒温恒容时,增加X的物质的量,平衡向正向移动,X的转化率提高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com