

| A. | 锌片为负极,稀硫酸是电解质溶液 | |
| B. | 电池工作时电子由锌片经导线流向铜片 | |
| C. | 电池工作时铜片逐渐溶解而质量减轻 | |
| D. | 电池工作时实现了化学能转化为电能 |
分析 铜锌原电池中,Zn易失电子作负极,Cu作正极,正极上氢离子得电子生成氢气,电子从负极流向正极,原电池是把化学能转化为电能的装置,据此分析解答.
解答 解:A.该原电池中,锌易失电子作负极,铜作正极,稀硫酸是电解质溶液,故A正确;
B.原电池中,负极失电子,则电子从负极流向正极,即电子从锌片流入铜片,故B正确;
C.Cu作正极,正极上氢离子得电子生成氢气,Cu的质量不变,故C错误;
D.原电池是把化学能转化为电能的装置,即电池工作时实现了化学能转化为电能,故D正确;
故选C.
点评 本题考查了原电池原理,根据电极上得失电子确定正负极,结合原电池概念来分析解答,题目难度不大,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 液氨可用作制冷剂 | B. | 氧化铝可用于制造耐火坩埚 | ||
| C. | 液态钠可作核反应堆的传热介质 | D. | 硅单质是光纤制品的基本原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、NO3-、Cl- | B. | K+、Mg2+、Na+、SO42- | ||
| C. | CO32-、K+、Cl-、Na+ | D. | Cu2+、NO3-、SO42-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
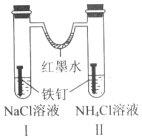
| A. | 红墨水水柱两边的液面变为左低右高 | |
| B. | I 和Ⅱ中负极反应式均为 Fe-2e-=Fe2+ | |
| C. | I 中正极反应式为 O2+2H2O+4e-=4OH | |
| D. | Ⅱ中 NH4Cl 溶液里有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 浓硫酸与乙醇170℃共热,制得的气体通入酸性KMnO4溶液 | 溶液紫色褪去 | 制得的气体为乙烯 |
| B | 测定等浓度的Na2CO3和Na2SO3的溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向2.0ml浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1AgNO3溶液,振荡 | 沉淀呈黄色 | Ksp(AgCl)>Ksp(AgI) |
| D | 向待测液中先滴加Ba(NO3)2溶液,再滴加稀盐酸 | 出现白色沉淀 | 原待测液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 除去CO2中的HCl气体 | 除去苯中的苯酚 | 观察铁的吸氧腐蚀 | 检验乙炔的还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CO2,溶液的pH 增大 | |
| B. | 升高温度,该平衡向右移动 | |
| C. | 加水,平衡正向移动,KW 增大 | |
| D. | 加入CH3COONa 固体,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 溶液中含NH4+ |
| B | 将石蜡油蒸气通过炽热的碎瓷片分解,得到的气体通入溴的四氯化碳溶液,溴的四氯化碳溶液褪色 | 分解产物中含乙烯 |
| C | 室温下,将BaSO4投入饱和Na2CO3溶液中充分反应,向过滤后所得固体中加入足量盐酸,固体部分溶解有无色无味气体产生 | Ksp(BaSO4)>Ksp(BaCO3) |
| D | 室温下,用pH试纸测得0.100mol•L-1 CH3COOH溶液的pH约为3,0.100mol•L-1 HCN溶液的pH约为5 | 酸性:HCN<CH3COOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com