
区分碳酸钠和碳酸氢钠固体的方法中(相同条件下),错误的是
A.加热,观察是否有气体放出
B.滴加稀盐酸,比较产生气体的快慢
C.溶于水后滴加氯化钙溶液,看有无沉淀
D.观察能否溶于水
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015届江西赣州市高二上学期期末联考化学试卷(解析版) 题型:填空题
工业上采用的一种污水处理方法是:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。某科研小组用此法处理污水,设计装置示意图,如图所示。
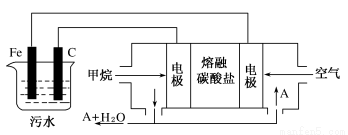
(1)实验时若污水中离子浓度较小,导电能力较差,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________。
A.BaSO4 B.CH3CH2OH C.Na2SO4 D.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:
①___________________________________________________;
②___________________________________________________。
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是__________ ____。
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。已知负极的电极反应是CH4 +4CO32--8e-=5CO2+2H2O。则正极的电极反应是 。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,此电池工作时必须有部分A物质参加循环,则A物质的化学式是_________。
查看答案和解析>>
科目:高中化学 来源:2015届江西省赣州市六校高二上学期期末联考化学试卷(解析版) 题型:选择题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- = 4OH -
B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S) -2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq)
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+
查看答案和解析>>
科目:高中化学 来源:2015届江西省新余市高二上学期期末考试化学试卷(解析版) 题型:选择题
0.1 mol/L K2CO3溶液中,若要使c(CO32-)更接近0.1 mol/L,可采取的措施是
A.加入少量盐酸 B.加KOH固体 C.加水 D.加热
查看答案和解析>>
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:实验题
为了“探究铁及其化合物的氧化性或还原性”.
(1)实验前同学预测:Fe2+肯定既有还原性又有氧化性.你认为他预测的依据是:__
(2)甲同学欲用实验证明他的预测.实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol·L -lFeCl2溶液、KSCN溶液、新制氯水.
①若计划在0.1 mol·L-l FeCl2溶液中滴入新制氯水,探究Fe2+的还原性,你预计可能发生反应的离子方程式为
②实验中,甲同学发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+反应的产物的存在以获取证据.你认为可选_____滴入小明所得的混合液中,并通过溶液出现___色的现象,证明该同学的观点和实验方案都是正确的.
③对于证明Fe2+具有氧化性,该同学认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果锌粒逐渐变小.由此说明三种金属的还原性由强至弱的顺序为_____ ___.
(3)甲同学分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为该同学梳理相关问题:若Fe2+在反应中表现出氧化性应转化成______(填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成_____.
②实际上Fe2+还原性较强,实验室的FeCl2溶液常因氧化而变质.除杂的方法是: ,相关反应的离子方程式:_____ .
查看答案和解析>>
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:选择题
下列实验方法正确的是
A.用CCl4萃取碘水后分液时,先打开分液漏斗活塞,放出下层液体,然后再从漏斗下口放出上层液体
B.用洁净铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定含有Na+
C.配制一定物质的量浓度的溶液时,若加水超过容量瓶的刻度线,用胶头滴管将多余液体吸出即可
D.检验某溶液中是否含有Fe3+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:选择题
下列离子在溶液中可大量共存,形成无色透明溶液的一组是
A.K+、Na+、OH—、MnO4- B.Ba2+、Cu2+、NO3—、SO42—
C.Mg2+、Na+、OH—、SO42— D.Cl—、Ba2+、NO3—、OH—
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二下学期学业水平模拟化学试卷(二)(解析版) 题型:选择题
下列实验方法不正确的是
A.用澄清石灰水鉴别Na2CO3和NaHCO3溶液
B.用焰色反应鉴别NaCl和KCl
C.用丁达尔效应鉴别硫酸钠溶液和硅酸胶体
D.用BaCl2溶液鉴别FeCl3溶液和Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(必修)(解析版) 题型:填空题
Ⅰ.合理饮食和正确用药,是人体健康的重要保证。
现有下列五种物质A食盐;B小苏打;C苹果汁;D葡萄糖;E青霉素,请按下列要求填空(填序号)。
富含维生素C的是 ,可直接进入血液,补充能量的是 ,应用最广泛的抗生素之一的是 ,既可作为疏松剂,又可治疗胃酸过多的是 ,食用过多会引起血压升高、肾脏受损的 。
Ⅱ.钢铁的生产与使用是人类文明和生活进步的一个重要标志。
(1)写出工业上用赤铁矿炼铁的主要化学反应方程式: 。
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:
①铁锅的腐蚀主要是由 (填化学或电化学)腐蚀造成的。形成的铁锈的主要成分是 。
②为防止轮船的船体在海水中腐蚀,一般在船身连接 (填“锌块”或“铜块”)。
Ⅲ.材料是人类赖以生存和发展的重要物质基础,合理使用材料可以改善我们的生活。
(1)体育场馆建设需大量建筑材料。下列材料不属于硅酸盐材料的是 (填字母)。
A.石灰石 B.水泥 C.玻璃
(2)在下列材料中,属于无机非金属材料的是 (填字母)。属于塑料制品的是 。
A.涤纶 B.聚氯乙烯塑料 C.氮化硅陶瓷 D.玻璃钢
(3)下列有关合金性质的说法正确的是 (填字母)。
A.合金的熔点一般比它的成分金属高
B.合金的硬度一般比它的成分金属低
C.组成合金的元素种类相同,合金的性能就一定相同
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
(4)合成塑料、合成橡胶和 是常说的三大合成材料。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com