
25℃时,等体积混合0.1mol/L的HCl溶液和0.06mol/L的Ba(OH)2溶液后,溶液的pH值等于( )
A.2.0 B.12.3 C.1.7 D.12.0
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源:2017届吉林省高三上11月模拟化学卷(解析版) 题型:选择题
下图是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
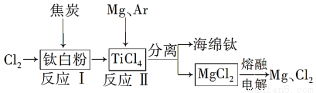
有关说法正确的是( )
A.反应Ⅰ中钛白粉做氧化剂
B.该工艺中可以循环使用的物质只有Cl2
C.可以用N2代替Ar作为反应Ⅱ中的保护气
D.反应Ⅱ的化学方程式为2Mg+TiCl4 2MgCl2+Ti
2MgCl2+Ti
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
常温下,有关①100ml 0.1 mol/L NaHCO3、②100ml 0.1 mol/L Na2CO3两种溶液的叙述不正确的是
A.均存在电离平衡与水解平衡 B.c(OH-):①>②
C.存在的粒子种类相同 D.②溶液中:c(HCO3-)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
下列物质中能抑制水的电 离且使溶液呈现出酸性的是
离且使溶液呈现出酸性的是
A.Na2CO3 B.Al2(SO4)3 C.K2SO4 D.H2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:实验题
实验室有一瓶混有少量NaCl杂质的NaOH固体试剂,为准确测其纯度,采用盐酸滴定法进行测定。
①称取WgNaOH固体试剂配制成100.00mL水溶液备用;
②将浓度为Cmol/L的标准盐酸装在用标准盐酸润洗过的25.00mL酸式滴定管中,调节液面位置在零刻度以下,并记下刻度;
③取V1 mL NaOH待测溶液置于洁净的锥形瓶中,加入2-3滴甲基橙指示剂充分振荡,然后用浓度为C mol/L的标准盐酸滴定,用去盐酸V2 mL,试回答:
(1)如有1mol/L和0.1mol/L的标准盐酸应选用___________mol/L盐酸,原因是______________。
(2)滴定终点的判断 。
(3)若酸式滴定管尖嘴气泡未排出,会使碱测定值__________(偏大、偏小、无影响)。
(4)不用标准盐酸润洗酸式滴定管,会使碱测定值__________(偏大、偏小、无影响)。
(5)固体试剂NaOH纯度计算式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
在体积固定的密闭容器中,加入2molA和1molB发生下列反应并且达到化学平衡状态,2A(g)+B(g)  3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
A.4molA+2molB B.3molC+1molB+1molD+1molA
C.2molA+1molB+1molD D.1molA+0.5molB + 1.5molC+0.5molD
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
已知H-H键能为436KJ/mol,H-N键能为391 KJ/mol,根据热化学方程式N2(g) +3H2(g) 2NH3(g) △H=-92.4kJ/mol。则N≡N的键能约为( )
2NH3(g) △H=-92.4kJ/mol。则N≡N的键能约为( )
A.431 kJ/mol B.946 kJ/mol C.649 kJ/mol D.896 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学试卷(解析版) 题型:选择题
通过以下反应均可获取H2。下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) ΔH1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=+206.1kJ·mol–1
A.反应①中太阳能转化为化学能
B.反应②为放热反应
C.反应③使用催化剂,ΔH3减小
D.反应CH4(g)=C(s)+2H2(g)的ΔH3= -74.8 kJ·mol–1
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:填空题
(1)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,Q与水反应的化学方程式为_____________。
(2)NaCN超标的电镀废水可用两段氧化法处理:
1.NaCN与NaClO反应,生成NaOCN和NaCl
2.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
①写出第二次氧化时发生反应的离子方程式。
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成____________和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO_________g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com