
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CBrCH(CH3)2 | D. | (CH3)2CHCH2CH2OH |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
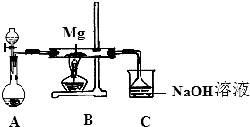 SiO2、SO2和CO2都是酸性氧化物,它们的化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.| 序号 | 实验步骤 | 预期现象和结论 |
| 1 | 取少量反应后所得固体于试管中 | |
| 2 | 向试管中的固体慢慢滴加2mol/L 盐酸至过量,试管口塞上导管的单孔塞,并将导管通入盛有品红的试管中 | 若试管中的固体完全溶解,则丙同学推测正确.若试管中的固体未完全溶解,且品红溶液褪色,则乙同学推测正确. |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向无色溶液中滴加氯水和CCl4,振荡静置 | 下层溶液显 紫色 | 原溶液中含有I- |
| B | 过量铁粉加入稀硝酸中充分反应,再加入KSCN溶液 | 溶液呈红色 | 稀硝酸将铁 氧化为Fe2+ |
| C | 向淀粉溶液中滴加稀硫酸,加热,取水解液少许,滴加银氨溶液,并水浴加热 | 没有银镜出现 | 淀粉没有发生水解 |
| D | 用玻璃棒蘸取浓硫酸滴到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 其中钠离子的浓度为0.2mol•L-1 | |
| B. | 溶液中的OH-浓度大于H+浓度,HCO3-的浓度小于CO32-的浓度 | |
| C. | 溶液中Na+的浓度等于CO32-浓度的二倍 | |
| D. | 溶液中H2CO3分子的浓度为0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com