
【题目】在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s)![]() CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
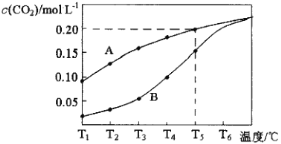
(1)该反应正反应为___(填“吸”或“放”)热反应,温度为T5℃时,该反应耗时40s达到平衡,则T5℃时,该反应的平衡常数数值为___。
(2)如果该反应的平衡常数K值变大,该反应___ (选填编号)。
a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)请说明随温度的升高,曲线B向曲线A逼近的原因:___。
(4)在T5℃下,维持温度和容器体积不变,向上述平衡体系中再充入0.5molN2,则最后平衡时容器中的CaCO3的质量为___ g。
(5)已知苯酚和碳酸的电离平衡常数如图所示。请写出二氧化碳通入苯酚钠溶液的化学反应离子方程式___,请用电离平衡原理解释上述反应发生的原因以及确定生成物的依据___。
物质 | 电离平衡常数(25℃) |
C6H5OH | Ki=1.28×10-10 |
H2CO3 | Ki1=4.3×10-7 |
Ki2=5.6×10-11 |
【答案】吸热 0.2 bc 随着温度升高,反应速率加快,达到平衡所需要的时间变短 10 C6H5O-+CO2+H2O→C6H5OH+HCO3- 二氧化碳与水结合生成碳酸,且碳酸酸性比苯酚酸性强,故能生成苯酚。碳酸的电离分两步:第一步:H2CO3![]() H++HCO3-,该步电离出的H+更容易结合C6H5O-生成酸性更弱的C6H5OH,导致第一步电离平衡正向移动,第二步电离:HCO3-
H++HCO3-,该步电离出的H+更容易结合C6H5O-生成酸性更弱的C6H5OH,导致第一步电离平衡正向移动,第二步电离:HCO3-![]() H++CO32-,C6H5OH酸性大于HCO3-,所以第二步电离出的H+更容易结合CO32-而不容易结合C6H5O-,故不影响第二步电离平衡
H++CO32-,C6H5OH酸性大于HCO3-,所以第二步电离出的H+更容易结合CO32-而不容易结合C6H5O-,故不影响第二步电离平衡
【解析】
(1)由图象判断温度与平衡移动的影响,再判断反应中的热效应;根据化学反应方程式可知,平衡常数K=c(CO2)计算;
(2)平衡常数增大,说明平衡正向移动,结合温度对平衡常数的影响判断;
(3)根据温度对反应速率的影响判断;
(4)由于容器体积不变,平衡体系中再充入0.5molN2,平衡不移动,据此计算;
(5)由电离平衡常数可知,苯酚的酸性弱于碳酸但比碳酸氢根强,据此答题。
(1)由图象可知,随着温度的升高,CO2平衡时的浓度增大,说明平衡向正反应方向移动,所以该反应为吸热反应。根据化学反应方程式可知,平衡常数K=c(CO2),所以T5℃时,K=c(CO2)=0.2;
(2)平衡常数增大,说明平衡正向移动,此时改变的条件为升高温度,如果该反应的平衡常数K值变大,则
a.一定向正反应方向移动,a错误;
b.在平衡移动时,由于是升高温度,所以正、逆反应速率都增大,由于该反应是吸热反应,所以平衡移动后温度会有所降低,所以正反应速率又逐渐减小,b正确;
c.一定向正反应方向移动,c正确;
d.根据b的分析可知,d错误;
故选bc;
(3)根据温度对反应速率的影响可知,随着温度升高,反应速率加快,达到平衡所需要的时间变短,所以曲线B向曲线A逼近;
(4)由于容器体积不变,平衡体系中再充入0.5molN2,平衡不移动,所以在T5℃时,n(CO2)=2L×0.2mol·L-1=0.4mol,则被分解的CaCO3的质量为100×0.4g=40g,所以平衡时容器中的CaCO3的质量为0.5mol×100g·mol-1-40g=10g;
(5)CO2入苯酚钠溶液的化学反应离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,由电离平衡常数可知,苯酚的酸性弱于H2CO3但比HCO3-强,CO2与H2O结合生成H2CO3,且H2CO3酸性比苯酚酸性强,故能生成苯酚,H2CO3的电离分两步:第一步:H2CO3![]() H++HCO3-,该步电离出的H+更容易结合C6H5O-生成酸性更弱的C6H5OH,导致第一步电离平衡正向移动,第二步电离:HCO3-
H++HCO3-,该步电离出的H+更容易结合C6H5O-生成酸性更弱的C6H5OH,导致第一步电离平衡正向移动,第二步电离:HCO3-![]() H++CO32-,C6H5OH酸性大于HCO3-,所以第二步电离出的H+更容易结合CO32-而不容易结合C6H5O-,故不影响第二步电离平衡。
H++CO32-,C6H5OH酸性大于HCO3-,所以第二步电离出的H+更容易结合CO32-而不容易结合C6H5O-,故不影响第二步电离平衡。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
A.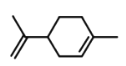 和
和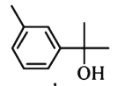 都属于芳香族化合物
都属于芳香族化合物
B. 和
和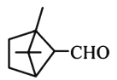 分子中所有碳原子均处于同一平面上
分子中所有碳原子均处于同一平面上
C. 、
、 和
和 均能使酸性
均能使酸性![]() 溶液褪色
溶液褪色
D. 和
和 均能与新制的
均能与新制的![]() 反应生成红色沉淀
反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.对于2HI(g)![]() H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深
B.合成氨反应中为提高氨的产率,理论上应采取降低温度的措施
C.实验室配制FeCl3溶液时,将FeCl3固体加入到少量的浓盐酸中再加水稀释
D.用饱和食盐水可以去除Cl2中的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A.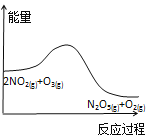 降低温度,平衡向正反应方向移动
降低温度,平衡向正反应方向移动
B. 0-3s内,反应速率v(NO2)=0.2mol·L-1
0-3s内,反应速率v(NO2)=0.2mol·L-1
C.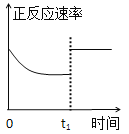 t1时仅加入催化剂,平衡正向移动
t1时仅加入催化剂,平衡正向移动
D.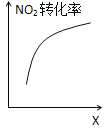 达到平衡时,仅改变X,则X为c(O2)
达到平衡时,仅改变X,则X为c(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素A、B、C、D、E原子序数依次增大。已知:A、C同主族,A的原子最外层电子数是次外层的3倍,B的氧化物既能溶于强酸,又能溶于强碱,D的原子半径是第3周期中最小的,E是形成骨骼和牙齿的主要元素,且E单质能和水反应。则下列分析错误的是
A. A的离子结构示意图为![]()
B. D的最高价氧化物的水化物的酸性大于C的最高价氧化物的水化物的酸性
C. E和D形成的离子化合物ED2的电子式为![]()
D. B的氧化物为离子化合物,只含离子键,其晶体为离子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锶(Sr)为第五周期第ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
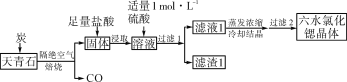
已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10
③SrCl2·6H2O的摩尔质量为267 g·mol-1
(1)工业上天青石焙烧前先研磨粉碎,其目的是___
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有硫元素被还原,转移了3 mol电子。写出该反应的化学方程式____
(3)加入硫酸的目的是_____;为了提高原料的利用率,滤液1中Sr2+的浓度应不高于__________mol·L-1(注:此时滤液1中Ba2+浓度为1×10-5 mol·L-1 )。
(4)滤渣1的主要成分是____________,滤液1经蒸发浓缩、冷却结晶、过滤后,需对所得的六水氯化锶晶体进行洗涤、干燥。证明六水氯化锶晶体已洗涤干净的实验操作及现象为___________
(5)工业上常通过电解熔融SrCl2制锶单质。由SrCl2·6H2O制取氯化锶的方法是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机样品(仅含C、H、O三种元素)3.0g在足量O2中完全燃烧,将燃烧后的混合物先通过足量的浓硫酸,浓硫酸增重1.8g,再通过足量的澄清石灰水,经过滤得到10g沉淀。该有机样品的组成可能是(括号内给出的是有机物的分子式)( )
A.葡萄糖(C6H12O6)与蔗糖(C12H22O11)
B.醋酸与甲酸甲酯(C2H4O2)
C.乙醇与甲醛(CH2O)
D.二甲醚(C2H6O)与乳酸(C3H6O3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A分子的立体结构图(其中C、H原子已去):因其分子中碳原子排列类似金刚石故名“金刚烷”,下列错误的是()
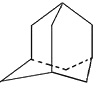
A. 金刚烷分子式是C10H16
B. 金刚烷分子的二氯代物有4种
C. 金刚烷分子中有4个六元环组成
D. 金刚烷分子的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合下图判断,下列叙述正确的是( )

A.Ⅰ和Ⅱ中正极均被保护
B.Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH-
D.Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com