
| A.反应②在任何温度下均能自发进行 |
| B.CO(g)+2H2(g)=CH3OH(g)△H>-90.5kJ/mol |
| C.甲醇的燃烧热为764kJ/mol |
| D.若CO的燃烧热为282.5kJ/mol,则H2的燃烧热为286kJ/mol |
科目:高中化学 来源:不详 题型:填空题
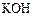 为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH
为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O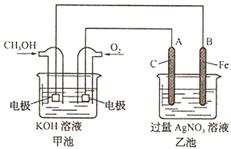
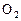 _________L(标准状况下)。
_________L(标准状况下)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该电池的正极是Zn,负极是Ag2O |
| B.该电池负极的电极反应式为:Zn+2OH——2e—=ZnO+H2O |
| C.理论上该电池工作一段时间后,溶液中KOH的浓度不变 |
| D.该电池工作时,电解质中的阴离子向负极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2PbSO4+2H2O 下列叙述正确的是( )
2PbSO4+2H2O 下列叙述正确的是( )| A.放电时PbO2是电池的负极,电解质溶液的密度逐渐减小 |
| B.放电时负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.电池充电时,PbO2得电子被氧化 |
| D.电池充电时,阴极电极反应式为:PbSO4+2H2O-2e-=PbO2+SO42-+4H- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
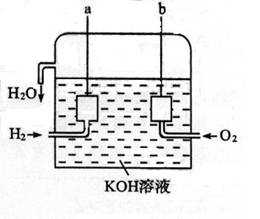
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
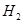 ②
②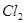 ③
③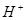 ④
④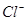 ⑤
⑤ ⑥
⑥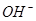
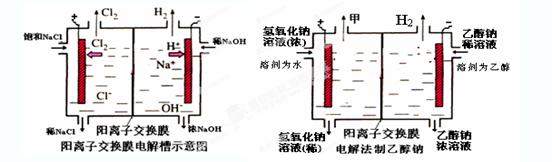
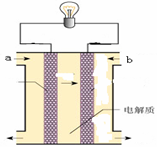
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Li2S2O4。下列说法正确的是( )
Li2S2O4。下列说法正确的是( )| A.该电池反应为可逆反应 |
| B.放电时,Li+向负极移动 |
| C.充电时,阴极反应式为Li++e一=Li |
| D.该电池的电解质溶液可以换成LiBr的水溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com