
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题

| A.储存H2的碳纳米管放电时为负极,充电时为阴极 |
| B.放电时负极附近pH减小 |
| C.放电时电池正极的电极反应为 NiO(OH)+H2O+e—===Ni(OH) 2+OH— |
| D.放电时,电池反应为2H2+O2===2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验编号 | 水果种类 | 电极间距离/㎝ | 电流大小/µA |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹 果 | 2 | 27.2 |

 __________。
__________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池是将化学能转化为电能的装置 |
| B.原电池中电子流入的一极是正极,发生氧化反应 |
| C.在氢—氧燃料电池中通入H2的一极是负极 |
| D.把铜片和锌片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 如下图所示。下列有关叙述正确的是
如下图所示。下列有关叙述正确的是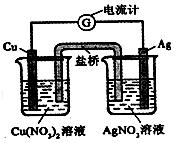
| A.在外电路中,电子由银电极流向铜电极 |
| B.取出盐桥后,电流计的指针仍发生偏转 |
| C.外电路中每通过0.1mol电子,铜的质量理论上减小6.4g |
| D.原电池的总反应式为Cu+2AgNO3==2Ag+Cu(NO3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com