
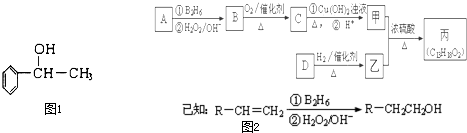
 ,乙为
,乙为 ,则丙为
,则丙为 ,据此解答.
,据此解答. ,乙为
,乙为 ,则丙为
,则丙为 ,
,| △ |
| △ |
 ,故答案为:
,故答案为: ;
;
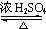
 +H2O,
+H2O,
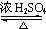
 +H2O;
+H2O; ,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为
,其同分异构体符合:苯环上有3个取代基或官能团,显弱酸性,则侧链为-OH、-CH3、-CH2CH3,若-CH3、-CH2CH3相邻,-OH有4种位置,若若-CH3、-CH2CH3相间,-OH有4种位置,若若-CH3、-CH2CH3相对,-OH有2种位置,故共有10种,苯环上 3个取代基或官能团互不相邻,则该同分异构体为 ,故答案为:10;
,故答案为:10; .
.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
A、Cu
| |||||
B、Cu
| |||||
C、Cu
| |||||
D、Cu
|
查看答案和解析>>
科目:高中化学 来源: 题型:

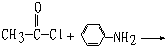
查看答案和解析>>
科目:高中化学 来源: 题型:
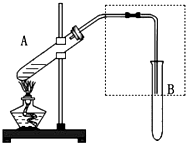 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
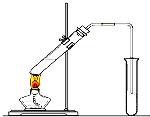 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| K+ | Na+ | NH4+ | SO42- | NO3- | Cl- | |
| 浓度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 50 |
| 1 |
| 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
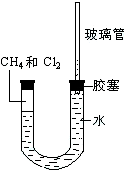 如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com