
下列与化学反应能量变化相关的叙述不正确的是( )
A.化学反应是旧键断裂和新键形成的过程
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH相同
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g,下列物质不能满足上述结果的是( )
A.CO B.H2
C.C6H12O6 D.C12H22O11
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数为________________。
在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合。
(1)若所得混合液为中性,且a=2,b=12,则VaVb=________。
(2)若所得混合液的pH=10,且a=2,b=12,则VaVb=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,H2(g)+CO2(g)H2O(g)+CO(g)的平衡常数K=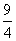 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)(mol·L-1) | 0.010 | 0.020 | 0.020 |
| c(CO2)(mol·L-1) | 0.010 | 0.010 | 0.020 |
下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol·L-1
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
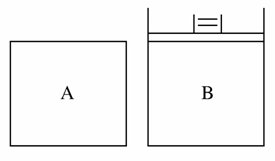
有A、B两容器(如图所示),A容积固定,B容积可变。一定温度下,在A中加2 mol N2、3 mol H2,发生反应:N2+3H22NH3,达平衡时生成NH3的物质的量为n。
(1)相同温度下,在B中充入4 mol N2、6 mol H2,当B的压强与A的压强相等,B中反应达平衡时,生成NH3的物质的量________2n(填“>”“<”或“=”,下同);当B的容积与A的容积相等,B中反应达平衡时,生成NH3的物质的量________2n。
(2)相同温度下,保持B的容积为A的一半,并加入1 mol NH3,要使B中反应达平衡时各物质的浓度分别与上述A容器中平衡时相同,则起始时应加入________mol N2和________mol H2。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O===O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为( )
A.920 kJ B.557 kJ
C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
按图①装置进行实验,若图中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是( )
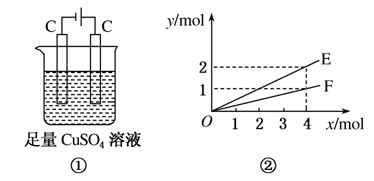
A.F表示反应生成Cu的物质的量
B.E表示反应实际消耗H2O的物质的量
C.E表示反应生成O2的物质的量
D.F表示反应生成H2SO4的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。下图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
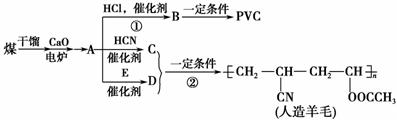
请回答下列问题:
(1)写出反应类型:反应①________,反应②________。
(2)写出结构简式:PVC________,C________。
(3)写出A―→D的化学反应方程式:_________________________________。
(4)与D互为同分异构体且可发生碱性水解的物质有____________种(不包括环状化合物),写出其中一种的结构简式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把①蔗糖 ②麦芽糖 ③淀粉 ④纤维素 ⑤油脂 ⑥酶 ⑦蛋白质,在酸存在的条件下分别进行水解,其水解的最终产物只有1种的有( )
A.①②③④⑤ B.②③④
C.④⑥⑦ D.③④⑤⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com