
【题目】BaTiO3、KH2PO4和NaNO2都属于铁电体,它们具有许多特异的性能如当它受压力而改变形状时产生电流,通电时会改变形状等。
(1)基态Ti原子的价电子排布式为___________,属于___________区元素。
(2)KH2PO4晶体中存在的作用力有___________(选填字母)。
A.离子键 B.共价键 C.氢键
(3) NaNO2中N原子的杂化类型为___,键角(填“>、<或=”)____120°,其原因是___________。N、O、Na三种元素的第二电离能(I2)由大到小的顺序为________(用元素符号表示)。
(4)BaTiO3的晶胞如下图所示:

Ti原子的配位数为_____,晶体的密度为ρg/cm3,最近的Ba原子和O原子之间的距离为___(填计算式)nm。( BaTiO3的摩尔质量为233g/mol,NA为阿伏加德罗常数的值)
【答案】3d24s2 d ABC sp2 < N原子上有一对孤对电子,孤电子对与成键电子对间的斥力大于成键电子对之间的斥力 Na>O>N 6 ![]() ×107
×107
![]()
【解析】
(1) Ti是22号元素,根据原子构造原理可得其核外电子排布式,得到基态Ti原子的价电子排布式,并根据元素原子结构与元素在周期表的位置关系判断其所属区域;
(2)KH2PO4是盐,属于离子晶体,含离子键,在阴离子H2PO4-中含有P=O键、O-H键,可形成氢键;
(3)根据N、O原子间形成的电子对分析原子杂化,并结合孤电子对与成键电子对之间的作用力情况判断键角大小;
(4)从元素的+1价离子的稳定性大小分析I2大小;
(5)根据晶胞在各种微粒的空间构型及相对位置判断Ti的配位体数目;用均摊法计算一个晶胞中含有的各种元素的原子个数,计算晶胞的质量,利用m=ρV、及边长V= L3计算晶胞边长,最后根据Ba与O原子的位置在面对角线的一半就可计算出两个微粒间的距离。
(1)Ti的原子序数为22,则基态原子的价电子排布式为3d24s2,位于第四周期IVB族,属于d区,故答案为3d24s2;d;
(2) KH2PO4是盐,属于离子晶体,含离子键,在阴离子H2PO4-中含有P=O键、2个O-H键,故可可形成氢键,故合理选项是ABC;
(3)NO2-的中心原子的价层电子对数为3,所以NO2-中的N原子采用sp2杂化,N原子的3个杂化轨道,其中一个被孤电子对占有,孤电子对与成键电子对间的斥力大于成键电子对之间的斥力,所以键角小于120°,故答案为sp2;<;N原子上有一对孤对电子,孤电子对与成键电子对间的斥力大于成键电子对之间的斥力;
(4) 由于Na+是最外层8个电子的稳定结构,气态基态Na+从8电子稳定结构再失去一个电子最难,气态基态O+从2p3半充满较稳定结构再失去一个电子较难。所以Na+ 的第二电离能I2最大,N+最小,因此三种元素的第二电离能(I2)由大到小的顺序为Na>O>N;
(5)根据晶胞结构示意图可知:Ti位于晶胞中心,O原子位于晶胞六个面心上,Ba位于晶体的8个顶点上,所以Ti的配位体数目是6;在一个晶胞中含有的各种元素的原子个数Ti:1×1=1;Ba:![]() ×8=1,O:
×8=1,O:![]() ×6=3,即一个晶胞中含有1个BaTiO3,其质量m=
×6=3,即一个晶胞中含有1个BaTiO3,其质量m=![]() g,由于晶胞的密度是ρg/cm3,所以晶胞的体积V=
g,由于晶胞的密度是ρg/cm3,所以晶胞的体积V=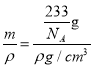 =
=![]() cm3,则晶胞的边长L=
cm3,则晶胞的边长L=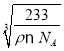 cm=
cm=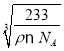 ×107nm,最近的Ba原子和O原子位于面对角线的一半位置,所以最近的Ba原子和O原子之间的距离为a=
×107nm,最近的Ba原子和O原子位于面对角线的一半位置,所以最近的Ba原子和O原子之间的距离为a=![]() L=
L=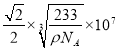 nm,故答案为6;
nm,故答案为6;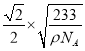 ×107。
×107。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】碳热还原氯化法从铝土矿中炼铝具有步骤简单、原料利用率高等优点,其原理如下:
Ⅰ.Al2O3(s) + AlCl3(g) + 3C(s) ![]() 3AlCl(g) + 3CO(g) – 1486 kJ
3AlCl(g) + 3CO(g) – 1486 kJ
Ⅱ.3AlCl(g) ![]() 2Al(l) + AlCl3(g) + 140 kJ
2Al(l) + AlCl3(g) + 140 kJ
(1)写出反应Ⅰ的化学平衡常数表达式K=_____________,升高温度,K_______(填增大、减小、不变)。
(2)写出反应Ⅱ达到平衡状态的一个标志_________________________________;结合反应Ⅰ、Ⅱ进行分析,AlCl3在炼铝过程中的作用可以看作___________。
(3)将1mol氧化铝与3mol焦炭的混合物加入2L反应容器中,加入2mol AlCl3气体,在高温下发生反应Ⅰ。若5min后气体总质量增加了27.6g,则AlCl的化学反应速率为_________ mol/(L·min)。
(4)Na2O2具有很强的氧化性。少量Na2O2与FeCl2溶液能发生反应:____Na2O2+ FeCl2+___H2O→____Fe(OH)3↓+_____FeCl3+____NaCl;已知FeCl2前面系数为6,配平上述化学方程式,并标出电子转移方向和数目________________。此反应中被还原的元素是____________,氧化产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的工艺流程如下:

则回答下列问题:
(1)操作1的名称为____________,用到的玻璃仪器除玻璃棒、烧杯外,还需_________;
(2)沉淀C的成分为________________(写化学式);
(3)设计最简实验证明滤液D中Fe3+已沉淀完全(写出操作、现象及结论,试剂任选):取2mL滤液D于试管中,__________________________。
(4)滤液E中的主要溶质的化学式为________________;
(5)写出步骤⑤的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 。向物质的量浓度相同的
。向物质的量浓度相同的![]() 和
和![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液产生
溶液产生![]() 、
、![]() 两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。
两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。
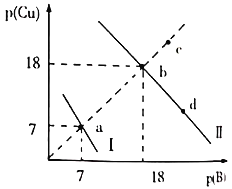
图中的![]() ,
,![]() 或
或![]() 。下列说法错误的是( )
。下列说法错误的是( )
A.曲线Ⅰ表示的是Cu2+与OH-浓度关系的曲线
B.该温度下,![]()
C.升高温度时,b点会向c点移动
D.向d点对应的溶液中加入对应阴离子的钠盐固体,d点向b点移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
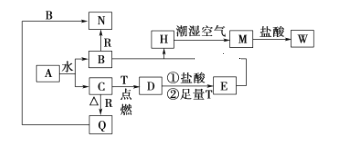
(1)写出下列物质的化学式A:_______________,Q:_____________,W:__________________。
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______________________
②R与B溶液反应时的离子方程式:___________________________________
③D与盐酸反应的离子方程式:_______________________________________
(3)简述检验气体C的方法:___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及硼的化合物有着广泛的用途。请回答下列问题:
(1)硼在元素周期表中的位置为____________,硼元素有两种天然同位素10B和11B,硼元素的近似相对原子质量为10.8,则两种同位素原子的原子个数之比为_____________。
(2)单质硼(B)在一定条件下与NaOH溶液反应生成NaBO2和一种气体,请写出该反应的化学方程式__________________________。
(3)硼酸(H3BO3)是一种白色片状晶体,微溶于水,对人体的受伤组织有着和缓的防腐消毒作用。硼酸是一元弱酸,室温时0.1mol/L硼酸的pH为5,计算硼酸的电离常数数K=____________。
氟硼酸(HBF4)是一种强酸,仅以离子状态存在于水中,请写出BF4-的电子式 ____________。
(4)B2H6是硼的一种气态氢化物,因组成与乙烷(C2H6)相似而被称为乙硼烷。
①经测定B2H6中B原子最外层也满足8电子结构,由此推测B2H6与C2H6分子结构____________(填“相同”或“不相同”)。
②B2H6可由BF3与NaBH4在一定条件下反应制得,写出该反应的化学方程式_____________。
③B2H6是强还原剂,它与水反应生成H3BO3和H2。若有0.1mol B2H6与水完全反应,则产生H2在标准状况下的体积为____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙3个烧杯中分别装有稀H2SO4、CuCl2溶液、饱和食盐水,甲中电极为锌片和铜片,乙中电极为石墨棒C1、C2,丙中电极为石墨棒C3、铁片,电极之间用导线相连。则下列叙述正确的是
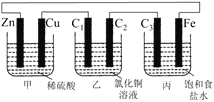
A.C1和C3放出的气体相同,铜片和铁片放出的气体也相同
B.C3是阴极,锌片、C2上都发生氧化反应
C.甲中H+向铜电极移动,丙中Cl-向铁电极移动
D.甲中硫酸溶液的浓度逐渐变小,丙中溶液的pH逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有___。
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4![]() 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
①该反应体现出酸性关系:H3PO4___H2SO4(填“>”或“<”)。
②结合元素周期律解释①中结论:P和S电子层数相同,___。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:__。
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:___。
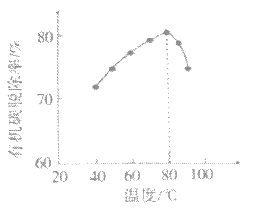
(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42-残留,加入BaCO3可进一步提高硫的脱除率,其离子方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
A.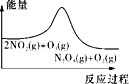 平衡后升温,NO2含量降低
平衡后升温,NO2含量降低
B.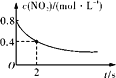 0~2 s内,v(O3)=0.2 mol·L-1·s-1
0~2 s内,v(O3)=0.2 mol·L-1·s-1
C.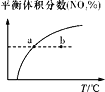 v正:b点>a点,b点:v逆 > v正
v正:b点>a点,b点:v逆 > v正
D.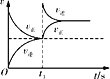 恒温,t1时再充入O3
恒温,t1时再充入O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com