
| A. | PCl3分子中三个共价键的键长相等 | |
| B. | PCl3分子中的P-Cl键属于极性共价键 | |
| C. | PCl3分子中三个共价键的键长、键角均相等 | |
| D. | PCl3分子中P-Cl键的三个键的键长相等,且属于极性分子 |
分析 A.PCl3分子中三个P-Cl键完全相同,所以键能、键长,键角都相等;
B.同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键;
C.PCl3分子中三个P-Cl键完全相同,所以键能、键长,键角都相等;
D.分子结构对称,为非极性分子,分子结构不对称,为极性分子.
解答 解:A.PCl3分子中三个P-Cl键完全相同,所以三个共价键的键长相等,但与三氯化磷分子空间构型是三角锥形而不是平面正三角形无关,故A错误;
B.不同非金属元素之间形成极性共价键,则分子中P-Cl键是极性共价键,但与三氯化磷分子空间构型是三角锥形而不是平面正三角形无关,故B错误;
C.PCl3分子中三个P-Cl键完全相同,所以键能相等,P-Cl键的三个键角都是100.1°,键角均相等,但与三氯化磷分子空间构型是三角锥形而不是平面正三角形无关,故C错误;
D.PCl3分子中P原子价层电子对数为4,采用sp3杂化,含有1个孤电子对,分子的空间构型是三角锥形,三角锥形分子的键角小于平面正三角形的键角,平面正三角形,则其键角应该为120°,已知PCl3分子中P-Cl键的三个键角都是100.1°,所以三氯化磷分子的空间构型是三角锥形而不是平面正三角形,即分子结构不对称,为极性分子为三氯化磷分子空间构型理由,故D正确;
故选D.
点评 本题考查了判断分子空间构型,不能根据选项叙述是否正确进行分析,确定三氯化磷分子的空间构型是三角锥形而不是平面正三角形理由的叙述为解答关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况) | 50 | 120 | 232 | 290 | 310 |
| A. | 在0~1,1~2,2~3,3~4,4~5min时间段中,反应速率最大的时间是4~5段,因为在此段时间内生成气体最多 | |
| B. | 在2~3min时间段内,用盐酸浓度变化表示的反应速率为0.1mol•L-1min-1 | |
| C. | 在该稀盐酸中分别加入等体积的蒸馏水、Na2SO4溶液或Na2CO3溶液都能减缓反应速率且不减少产生氢气的量 | |
| D. | 为了加快该化学反应速率,可以向其中加入MgSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
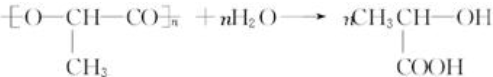 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “煤的液化”是指将煤加热变为液态 | |
| B. | “乙醇汽油”是为了增大燃烧的热值,在汽油中加入乙醇 | |
| C. | 光伏发电要用到铟,该元素是一种副族的金属元素 | |
| D. | 将燃料的燃烧反应设计为原电池,可以提高能量的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H6+C2H5Cl→C6C5-C2H5+HCl | |
| B. | C6H6+C2H5OH→C6H5-C2H5+H2O | |
| C. | C6H6+CH2=CH2→C6H5-C2H5 | |
| D. | C6H5-CH2CH2Br→C6H5-CH=CH2+HBr;C6H5-CH=CH2+H2→C6H5C2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气和水的反应:C12+H2O=2H++Cl-+ClO- | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 硫酸与氢氧化钡溶液反应:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸钡为强酸强碱的难溶性盐,俗名叫重晶石.
硫酸钡为强酸强碱的难溶性盐,俗名叫重晶石.| 反应温度 | 300℃ | 400℃ | 500℃ | 600℃ | 700℃ |
| 平衡常数 | 3.8 | 5.7 | 8.5 | 9.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com