
【题目】实验室用氢氧化钠固体配制1.00mol·L-1的NaOH溶液500mL,回答下列问题。
(1)关于容量瓶的使用,下列操作正确的是________(填字母)。
a.使用前要检验容量瓶是否漏液
b.用蒸馏水洗涤后必须要将容量瓶烘干
c.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
d.为了使所配溶液浓度均匀,定容结束后,要摇匀
e.用500mL的容量瓶可以直接配制480mL溶液
f.当用容量瓶配制完溶液后,可用容量瓶存放所配制的试剂
(2)请补充完整实验的简要步骤。
①计算;②称量NaOH固体________g;③溶解;④冷却并移液;⑤洗涤并转移;⑥________;⑦摇匀。
(3)本实验用到的基本仪器已有烧杯、天平(带砝码)、镊子、量筒、玻璃棒,还缺少的仪器是________、________。
(4)上述实验操作②③都要用到小烧杯,其作用分别是_____________________和_______。
(5)如图是该同学转移溶液的示意图,图中有两处错误,请写出:
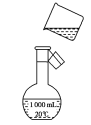
①____________________________________________;
②_____________________________________________。
(6)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________(填字母)。
A.转移溶液时不慎有少量液体洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀,静置后,发现液面低于刻度线,再加水至刻度线
【答案】ad 20.0 定容 500mL容量瓶 胶头滴管 用烧杯称量NaOH固体,防止NaOH腐蚀天平的托盘 用烧杯做溶解用的容器 没有用玻璃棒引流 应选用500mL的容量瓶 BC
【解析】
(1)a、容量瓶使用前要检验是否漏水,a正确;
b、容量瓶不能加热,b错误;
c、容量瓶不可以用来稀释浓溶液,也不能用来溶解固体,c错误;
d、为了使所配溶液浓度均匀,定容结束后要摇匀,d正确;
e、用500mL的容量瓶只能配制500mL溶液,不能配制480mL溶液,e错误;
f、容量瓶不能长期贮存溶液,f错误;
故选ad;
(2)m(NaOH)=nM=cVM=1.00mol·L-1×0.500L×40g·mol-1=20.0g。配制时,要遵循计算、称量、溶解(冷却)、移液、洗涤、定容、摇匀的顺序进行配制。
(3)配制一定物质的量浓度溶液使用的仪器有一定规格的容量瓶、烧杯、玻璃棒、胶头滴管、托盘天平(带砝码)、量筒,本题还缺少500mL容量瓶和胶头滴管。
(4)NaOH固体具有强腐蚀性,不能用纸称量,要用玻璃仪器(如小烧杯)盛放。NaOH固体溶解时要在小烧杯中进行。
(5)配制500mL的溶液,应选用500mL的容量瓶;在转移溶液时,一定要用玻璃棒引流,防止溶液溅到瓶外。
(6)A、转移溶液时不慎有少量液体洒到容量瓶外面,导致溶质损失,则所配溶液浓度偏低,A错误;
B、定容时俯视液面,则溶液体积偏小,导致所配溶液浓度偏高,B正确;
C、在未降至室温时,立即将溶液转移至容量瓶定容,则冷却后溶液体积偏小,导致所配溶液浓度偏高,C正确;
D、定容后,加盖倒转摇匀后,由于会有少量液体残留在刻线上方,因此液面低于刻度线是正常的,又滴加蒸馏水至刻度,体积会增大,导致所配溶液浓度偏低,D错误;
故选BC。


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式:2NO+2CO 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) /mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO) /mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)若1molNO和1molCO的总能量比1molCO2和0.5molN2的总能量大,则上述反应的![]() ___0(填写“>”、“<”、“=”)。
___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)计算4s时NO的转化率为____________。
(4)下列措施能提高NO和CO转变成CO2和N2的反应速率的是______(填序号)。
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(5)由上表数据可知,该反应在第______s达到化学平衡状态。假如上述反应在密闭恒容容器中进行,判断该反应是否达到平衡的依据为________(填序号)。
A.压强不随时间改变B.气体的密度不随时间改变
C.c(NO)不随时间改变D.单位时间里消耗NO和CO的物质的量相等
(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
Ⅰ | 280 | 1.20×10-3 | 82 | |
Ⅱ | 5.80×10-3 | 124 | ||
Ⅲ | 350 | 124 |
①请在上表格中填入剩余的实验条件数据_____、_____、______、______、______。
②请在给出的坐标图中,画出上表中的Ⅰ、Ⅱ两个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________。
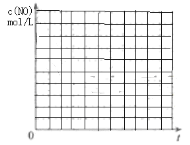
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种强电解质,它们溶于水在水中电离出的阳离子有K+、Ag+,阴离子有NO3-、OH-(电解质电离的离子有重复)。
图1装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为铂电极。接通电源,经过一段时间后,测得甲中b电极质量增加了43.2 g。常温下各烧杯中溶液pH与电解时间t关系如图2。请回答下列问题:
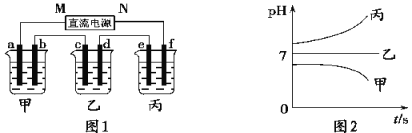
(1)写出三种强电解质的化学式:A____________;B____________;C____________。
(2)写出甲烧杯中总反应的化学方程式___________________________________________。
(3)若甲烧杯中溶液体积为400 mL(忽略溶液体积的变化) ,电解一段时间后甲烧杯溶液的pH=_______,丙烧杯e电极上生成的气体在标准状况下的体积为_______________。
(4)若直流电源使用的是铅蓄电池,铅蓄电池的正极材料是PbO2,负极材料是Pb,电解质溶液是H2SO4溶液,则放电时M极上发生的电极反应为_____________________________________。铅蓄电池充电时,若阳极和阴极之间用阳离子交换膜(只允许H+通过)隔开,则当外电路通过0.2 mol电子时,由阳极室通过阳离子交换膜进入阴极室的阳离子有________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着能源技术的发展,科学家们将目光聚焦于锂的开发与研究。
(1)锂元素的性质与原子结构密切相关。写出锂的原子结构示意图:______。
(2)根据元素周期律推断:
①锂与水反应的化学方程式是_______。
②在碱金属元素的最高价氧化物对应的水化物中, LiOH的碱性最_______(填“强”或“弱”)。
(3)已知:M(g) → M+(g)+e- H(M代表碱金属元素)
元素 | Li | Na | K | Rb | Cs |
H(kJ/mol) | +520 | +496 | +419 | +403 | +376 |
①根据以上数据,元素的金属性与H的关系是_________。
②从原子结构的角度解释①中结论:__________。
(4)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如下图所示:
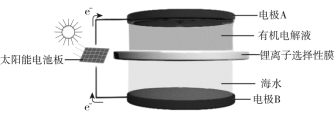
①金属锂在电极______(填“A”或“B”)上生成。
②阳极产生两种气体单质,电极反应式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向乙酸、乙醇、乙酸乙酯和水的平衡体系中加入少量含有18O的![]() ,达到新平衡后,体系中含有18O的物质是
,达到新平衡后,体系中含有18O的物质是
A. 乙酸、乙醇 B. 乙醇、乙酸乙酯
C. 乙醇、乙酸乙酯和水 D. 乙酸、乙醇、乙酸乙酯和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇广泛存在于食物(例如桑甚、花生,尤其是葡萄)中,它可能具有抗癌性。能够与1 mol该化合物发生反应的Br2和H2的最大用量分别是( )
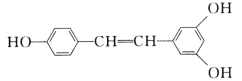
A.1mol、1molB.3.5mol、7mol
C.3.5mol、6molD.6mol、7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对牙膏中物质的探究要用到许多化学知识。
(1)下表列出了三种牙膏中的摩擦剂,请在表中填写三种摩擦剂所属的物质类别:
牙膏 | 两面针牙膏 | 佳洁士牙膏 | 中华牙膏 |
摩擦剂 | 氧化镁(MgO) | 碳酸钙(CaCO3) | 二氧化硅 (SiO2) |
摩擦剂的物质类别(指酸、碱、盐、酸性氧化物、碱性氧化物) | _________ | _________ | _________ |
(2)根据推测,牙膏摩擦剂的溶解性是_________(填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某学生设计了一种实验室制备碳酸钙的实验方案,其流程图如下:
石灰石![]() 生石灰
生石灰![]() 石灰水
石灰水![]() 碳酸钙
碳酸钙
请写出上述方案中有关反应的化学方程式:
①___________________ ③___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuO | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com