
| 选项 | 实验器材 | 相应实验 |
| A | 试管、铁架台、导管、酒精灯 | 乙酸乙酯的制备 |
| B | 锥形瓶、漏斗、双孔塞、导管、带余烬的木条、药匙 | 检验MnO2对H2O2分解速率的影响 |
| C | 500mL容量瓶、烧杯、玻璃棒、天平 | 配制 500mL1.00mol/LNaCl溶液 |
| D | 三脚架、坩埚、酒精灯、坩埚钳 | 钠在空气中燃烧 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.在试管中发生乙酸与乙醇的酯化反应,反应需要加热;
B.气体可能从漏斗逸出,且需要针筒测定气体的体积,需要秒表测定时间;
C.在烧杯中溶解、冷却后转移到容量瓶中定容;
D.在坩埚中灼烧钠.
解答 解:A.在试管中发生乙酸与乙醇的酯化反应,反应需要加热,则试管、铁架台、导管、酒精灯可完成酯化反应,故A正确;
B.气体可能从漏斗逸出,且需要针筒测定气体的体积,需要秒表测定时间,缺少必要的仪器,不能测定分解速率,故B错误;
C.在烧杯中溶解、冷却后转移到容量瓶中定容,则缺少胶头滴管,不能完成溶液配制,故C错误;
D.在坩埚中灼烧钠,则三脚架、坩埚、酒精灯、坩埚钳,泥三角为配套仪器,缺少泥三角不能完成钠的燃烧实验,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、制备实验、仪器的使用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| X | Y | W | Q | |
| 10min | 1.0mol | 3.0mol | 1.0mol | 2.0mol |
| 20min | 0.5mol | 1.5mol | 2.0mol | 1.0mol |
| A. | X+2Y═2W+2Q | B. | 3X+Y+2W═2Q | C. | X+3Y+2Q═2W | D. | X+2Y+3Q═2W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消除硫酸厂尾气排放:SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | 治理汽车尾气中NO和CO,可利用催化装置将NO与CO转化成CO2和N2 | |
| C. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| D. | 制CuSO4:2Cu+O2 $\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO CuO+H2SO4═CuSO4+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物的熔沸点都比较低 | |
| B. | 氢的三种核素可组成6种水分子 | |
| C. | H2O分子比H2S分子稳定的原因,是H2O分子间存在氢键 | |
| D. | SiO2和CaCO3在高温下反应生成CO2气体,说明硅酸的酸性比碳酸强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe与过量稀HNO3反应,电子转移数为2NA | |
| B. | 120g由NaHSO4和KHSO3组成的混合物含硫原子数为NA | |
| C. | 标准状况下,22.4LCH2Cl2含氯原子数为2 NA | |
| D. | 0.3mol/LAl(NO3)3溶液中含A13+数小于0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 苯甲醛 | 苯甲酸 | 苯甲醇 | |
| 沸点/℃ | 178.1 | 249.2 | 205.4 |
| 熔点/℃ | -26 | 121.7 | -15.3 |
| 溶解性 ( 常温 ) | 微溶于水,易溶于有机溶剂 | ||
| A. | 苯甲醛既发生了氧化反应,又发生了还原反应 | |
| B. | 可用银氨溶液判断反应是否完全 | |
| C. | 反应后的溶液先用分液法分离出有机层,再用蒸馏法分离出苯甲醇 | |
| D. | 反应后的溶液中加酸、酸化后,用过滤法分离出苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现 丁达尔效应 | 产生了 Fe(OH)3胶体 |
| B | 向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| C | 将溴乙烷和NaOH的乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
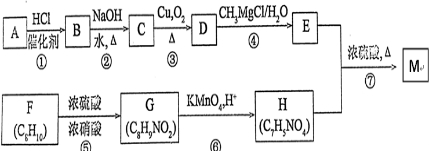
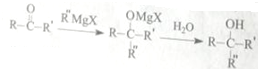
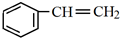 ,H中官能团的名称为羧基、硝基.
,H中官能团的名称为羧基、硝基.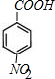 +
+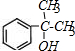 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、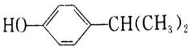 .(任写一种)
.(任写一种)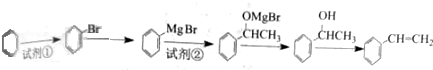
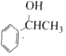 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$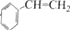 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com