
| A£® | “Ė·“Ó¦²»ŹōÓŚ»Æѧ±ä»Æ | |
| B£® | 112 ŗÅŌŖĖŲµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ 227 | |
| C£® | æĘѧ¼ŅŗĻ³ÉµÄ 112 ŗÅŌŖĖŲµÄŌ×ÓµÄÖŠ×ÓŹżĪŖ 165 | |
| D£® | 112 ŗÅŌŖĖŲŹōÓŚµŚĘßÖÜĘŚŌŖĖŲ |
·ÖĪö 112ŗÅŌŖĖŲµÄŌ×Ó£¬øĆŌŖĖŲŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ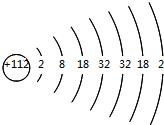 £¬øł¾ŻĘäŌ×Ó½į¹¹Ź¾ŅāĶ¼ÖŖ£¬øĆŌŖĖŲĪ»ÓŚµŚ7ÖÜĘŚµŚIIB×壬ĘäÖŠ×ÓŹż=ÖŹĮæŹż-ÖŠ×ÓŹż£¬¾Ż“Ė·ÖĪö½ā“š£®
£¬øł¾ŻĘäŌ×Ó½į¹¹Ź¾ŅāĶ¼ÖŖ£¬øĆŌŖĖŲĪ»ÓŚµŚ7ÖÜĘŚµŚIIB×壬ĘäÖŠ×ÓŹż=ÖŹĮæŹż-ÖŠ×ÓŹż£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ“Ė112 ŗÅŌŖĖŲŌ×ÓÖŠ×ÓŹż=70+208-1=277
A£®“Ė·“Ó¦Ō×ÓŗĖ·¢ÉśĮĖøı䣬ŹōÓŚŗĖ·“Ó¦²»ŹōÓŚ»Æѧ±ä»Æ£¬¹ŹAÕżČ·£»
B£®“Ė112 ŗÅŌŖĖŲŌ×ÓÖŠ×ÓŹż=70+208-1=277£¬Ļą¶ŌŌ×ÓÖŹĮæŌ¼µČÓŚÖŹĮæŹż£¬¹ŹB“ķĪó£»
C£®112 ŗÅŌŖĖŲŌ×ÓÖŠ×ÓŹż=277-112=165£¬¹ŹCÕżČ·£»
D£®øł¾ŻĘäŌ×Ó½į¹¹Ź¾ŅāĶ¼ÖŖ£¬øĆŌŖĖŲĪ»ÓŚµŚ7ÖÜĘŚµŚIIB×壬¹ŹDÕżČ·£®
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌ×Ó½į¹¹ŗĶŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ£¬ŹģĻ¤ŌŖĖŲÖÜĘŚ±ķ½į¹¹ŹĒ½ā±¾Ģā¹Ų¼ü£¬øł¾ŻŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČ·¶ØĘäŠŌÖŹ£¬ÖŖµĄÖŹĮæŹż”¢ÖŠ×ÓŹż”¢ÖŹ×ÓŹżµÄ¹ŲĻµ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CaO+H2O=Ca£ØOH£©2 | B£® | 2Na2O2+2H2O=4NaOH+O2”ü | ||
| C£® | 2Na+2H2O=2NaOH+H2”ü | D£® | 4Fe£ØOH£©2+2H2O+O2=4Fe£ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Ca2+”¢OH-”¢HCO3- | B£® | Fe2+”¢H+”¢CO32-”¢Cl- | ||
| C£® | Mg2+”¢NH4+”¢Cl-”¢SO42- | D£® | K+”¢Fe3+”¢NO3-”¢SCN- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
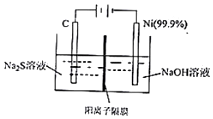 ĻÖ“śĆŗ»Æ¹¤²śÉśµÄH2SŹĒŅ»ÖÖÖŲŅŖµÄ¹¤Ņµ×ŹŌ“£®Ēė»Ų“š£ŗ
ĻÖ“śĆŗ»Æ¹¤²śÉśµÄH2SŹĒŅ»ÖÖÖŲŅŖµÄ¹¤Ņµ×ŹŌ“£®Ēė»Ų“š£ŗ| ·Ö×Ó | COS | H2 | H2O | CO | H2S | CO2 |
| ÄÜĮæ/KJ/mol | 1323 | 436 | 926 | X | 678 | 1606 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗµÄ pH Öš½„Ōö“ó | B£® | ČÜŅŗÖŠµÄ c£ØOH-£©Öš½„¼õŠ” | ||
| C£® | “×ĖįµÄµēĄė³Ģ¶ČÖš½„Ōö“ó | D£® | ČÜŅŗµÄµ¼µēÄÜĮ¦Öš½„¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē¼«²ÄĮĻ Fe”¢Cu£¬µē½āÖŹČÜŅŗ FeCl3 ČÜŅŗ | |
| B£® | µē¼«²ÄĮĻŹÆÄ«”¢Cu£¬µē½āÖŹČÜŅŗ Fe2£ØSO4£©3ČÜŅŗ | |
| C£® | µē¼«²ÄĮĻ Pt”¢Cu£¬µē½āÖŹČÜŅŗ FeCl3ČÜŅŗ | |
| D£® | µē¼«²ÄĮĻ Ag”¢Cu£¬µē½āÖŹČÜŅŗ Fe2£ØSO4£©3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéŗĶŅŅĻ©¶¼æÉŅŌŹ¹äåĖ®ĶŹÉ« | |
| B£® | ŅŅ“¼ŗĶŅŅĖį¶¼“ęŌŚĢ¼ŃõĖ«¼ü | |
| C£® | øßĆĢĖį¼ŲĖįŠŌČÜŅŗ²»æÉŅŌŃõ»Æ±½ŗĶ¼×Ķé | |
| D£® | ŅŅĻ©æÉŅŌÓėĒāĘų·¢Éś¼Ó³É·“Ó¦£¬±½²»ÄÜÓėĒāĘų¼Ó³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | .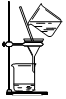 ×°ÖĆæÉÓĆÓŚ³żČ„ŅŅ“¼ÖŠµÄäå±½ | |
| B£® | .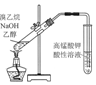 ÓĆĶ¼ĖłŹ¾×°ÖĆ¼ģŃéäåŅŅĶéÓėNaOH“¼ČÜŅŗ¹²ČČ²śÉśµÄC2H4 | |
| C£® | .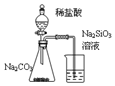 ×°ÖĆæÉÖ¤Ć÷·Ē½šŹōŠŌCl£¾C£¾Si | |
| D£® | 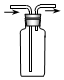 ×°ÖĆæÉÓĆÓŚŹÕ¼ÆO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
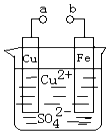
| A£® | aŗĶb²»Į¬½ÓŹ±£¬ĢśĘ¬ÉĻ»įÓŠ½šŹōĶĪö³ö | |
| B£® | aŗĶbÓƵ¼ĻßĮ¬½ÓŹ±£¬ĢśĘ¬ÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗFe-3e-ØTFe3+ | |
| C£® | ĪŽĀŪaŗĶbŹĒ·ńĮ¬½Ó£¬ĢśĘ¬¾ł»įČܽā£¬ČÜŅŗ“ÓĄ¶É«Öš½„±ä³ÉĒ³ĀĢÉ« | |
| D£® | aŗĶbÓƵ¼ĻßĮ¬½Óŗó£¬ĢśĘ¬ÉĻ·¢Éś»¹Ō·“Ó¦£¬ČÜŅŗÖŠĶĄė×ÓĻņĶµē¼«ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com