
| A、4 g重水(D2O)中所含中子数为0.2NA |
| B、4.48 L H2和O2的混合气体中所含分子数为0.2NA |
| C、0.2 mol Cl2溶解于等体积的水中,转移电子数为0.2NA |
D、12.6 g三聚氰胺(结构如右图)所含碳氮单键的数目为0.6NA |
| m |
| M |


科目:高中化学 来源: 题型:
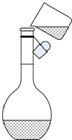 实验室中需要配制500mL0.10mol/L的NaOH溶液.回答下列问题.
实验室中需要配制500mL0.10mol/L的NaOH溶液.回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将水沿器壁慢慢注入浓硫酸中,并不断搅拌 |
| B、蒸发溶液时有液体飞溅,应立即加水冷却 |
| C、将酒精灯熄灭后,再向其中补充酒精至适量 |
| D、金属钠、钾着火时,应立即用沙子或湿抹布扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Mg2+、SO42-、OH- |
| B、Ba2+、K+、SO42-、NO3- |
| C、H+、K+、Cl-、HCO3- |
| D、Fe3+、K+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三者浓度相同时,pH大小顺序为③>②>① |
| B、三者浓度相同时,稀释相同倍数,pH变化最大的为② |
| C、三者的pH均为9时,物质的量浓度的大小关系为③>②>① |
| D、三者浓度相同时,分别加入同体积同浓度的盐酸后,pH最大的是① |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、①②③④⑤ |
| C、③④ | D、②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com