
 计算乙醇和水的物质的量,每个乙醇分子和水分子都含有1个氧原子,
计算乙醇和水的物质的量,每个乙醇分子和水分子都含有1个氧原子,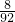 ,据此计算氢元素质量,根据n=
,据此计算氢元素质量,根据n= 计算氢原子的物质的量,根据氢原子守恒计算水的物质的量,根据N=nNA计算水分子数目.
计算氢原子的物质的量,根据氢原子守恒计算水的物质的量,根据N=nNA计算水分子数目. .
. 计算重水的物质的量,每个水分子含有10个质子,根据N=nNA计算质子数目.
计算重水的物质的量,每个水分子含有10个质子,根据N=nNA计算质子数目.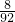 ,所以92gC3H8O3和C7H8的混合物中氢元素的质量为92g×
,所以92gC3H8O3和C7H8的混合物中氢元素的质量为92g×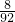 =8g,氢原子的物质的量为
=8g,氢原子的物质的量为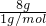 =8mol,所以生成水的物质的量为4mol,水分子数目为4mol×NAmol-1=4NA,故B正确;
=8mol,所以生成水的物质的量为4mol,水分子数目为4mol×NAmol-1=4NA,故B正确; ,0.1mol石墨晶体中存在的C-C键数目为0.1mol×3×
,0.1mol石墨晶体中存在的C-C键数目为0.1mol×3× ×NAmol-1=0.15NA,故C错误;
×NAmol-1=0.15NA,故C错误; =0.9mol,每个水分子含有10个质子,所以含有质子数为0.9mol×10×NAmol-1=9NA,故D正确.
=0.9mol,每个水分子含有10个质子,所以含有质子数为0.9mol×10×NAmol-1=9NA,故D正确.

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com