
【题目】下列变化中离子键被破坏的是( )
A. 氯化氢溶于水 B. 石墨转化为金刚石
C. 钠在氯气中燃烧 D. 加热氯化钠至熔化
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管已部分变质的一定质量的NaHCO3样品溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不计溶于水的CO2气体)

试求:
(1)该盐酸溶液的物质的量浓度为_______mol·L-1。
(2)未变质前NaHCO3的物质的量为 ________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在溶液中能够大量共存,当溶液中c(H+)=1×10-1mol·L-1时,有气体产生,而当溶液中c(H+)=1×10-13 mol·L-1时,又能生成沉淀。则该组离子可能为( )
A. HCO![]() 、Na+、Al3+、NO
、Na+、Al3+、NO![]() B. Fe2+、Na+、SO
B. Fe2+、Na+、SO![]() 、NO
、NO![]()
C. Mg2+、NH![]() 、SO
、SO![]() 、Cl- D. Na+、MnO
、Cl- D. Na+、MnO![]() 、NO
、NO![]() 、S2-
、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
①将金属Na投入水中:2Na+2H2O=2Na++2OH-+H2↑
②在硫酸溶液中加入氢氧化钡溶液至中性:Ba2++OH-+H++SO2-4=BaSO4↓+H2O
③碳酸氢钠溶液中滴加盐酸:HCO3-+H+=CO2↑+H2O
④氢氧化钠中滴加醋酸:OH-+H+=H2O
A. ①③④ B. ①③ C. ②④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素的性质及其递变规律正确的是( )
A. 第二周期元素从左到右,最高正价从+1递增到+7
B. 同一主族的元素,原子半径越大,越容易失去电子,其单质的氧化性越强
C. 最外层电子数比次外层电子数多的元素一定位于第二周期
D. 碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
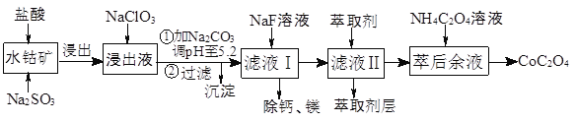
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:
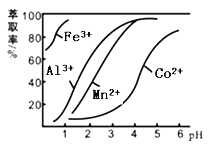
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
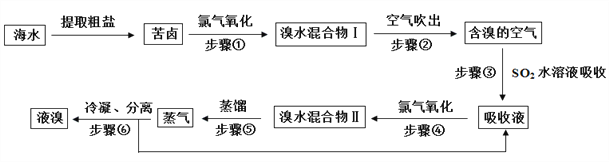
(1)步骤①获得Br2的离子反应方程式为:________________________________________;
(2)步骤③所发生反应的化学方程式为:________________________________________。在该反应中,氧化剂是______________(填化学式);若反应中生成2molHBr,则转移电子数约为_____________个。
(3)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是:_______________
(4)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(5)提取溴单质时,蒸馏溴水混合物Ⅱ而不是蒸馏溴水混合物Ⅰ,请说明原因:________________。(6)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法不正确的是

A. 在铝土矿制备较高纯度A1的过程中常用到NaOH溶液、CO2气体、冰晶石
B. 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C. 在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D. 黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.B两主族元素位于同一周期,它们的原子能以共价键结合成化学式为AB2的分子,A、B元素在周期表中的族序数可能为
A. ⅠA、ⅤA B. ⅠA、ⅦA C. ⅣA、ⅥA D. ⅡA、ⅦA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com