
【题目】乙醇是重要的有机化工原料,也是优质的燃料,工业上可由乙烯水合法或发酵法生产。回答下列问题:
(1)乙烯水合法可分为两步
第一步:反应CH2=CH2+ HOSO3H(浓硫酸)→CH3CH2OSO3H(硫酸氢乙酯);
第二步:硫酸氢乙酯水解生成乙醇。
①第一步属于反应_______________(填反应类型)。
②第二步反应的化学方程式为_____________________________。
(2)发酵法制乙醇,植物秸秆(含50%纤维素)为原料经以下转化制得乙醇
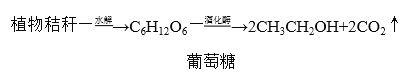
纤维素的化学式为________,现要制取4.6 吨乙醇,至少需要植物秸秆________吨。
(3)乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。乙醇汽油中乙醇是可再生能源,来源于________(填“乙烯水合法”或“发酵法”)。
(4)以乙醇为原料可制备某种高分子涂料,其转化关系如下图:

①有机物A的结构简式为___________。
②反应Ⅱ的化学方程式为___________。
③反应Ⅱ的反应类型为___________。
【答案】加成反应CH3CH2OSO3H+H2O→CH3CH2OH+H2SO4(C6H10O5)n16.2发酵法CH2=CHCOOHnCH2=CHCOOC2H5![]()
![]() 加聚反应
加聚反应
【解析】
(1)①乙烯含有碳碳双键,与硫酸发生加成反应生成硫酸氢乙酯;
②硫酸氢乙酯水解生成乙醇,根据原子守恒可知还有硫酸生成,则第二步反应的化学方程式为CH3CH2OSO3H+H2O→CH3CH2OH+H2SO4。
(2)纤维素的化学式为(C6H10O5)n,根据方程式可知(C6H10O5)n~nC6H12O6~2nCH3CH2OH,则要制取4.6吨乙醇,至少需要植物秸秆的质量是![]() 。
。
(3)由于乙醇汽油中乙醇是可再生能源,而乙烯是通过石油的裂解产生的,石油是不可再生的,所以来源于发酵法。
(4)①乙醇和A反应生成CH2=CHCOOC2H5,该反应是酯化反应,所以根据原子守恒可知A是CH2=CHCOOH;
②CH2=CHCOOC2H5含有碳碳双键,能发生加聚反应生成高分子化合物,则反应Ⅱ的化学方程式为nCH2=CHCOOC2H5![]()
![]() ;
;
③根据以上分析可知反应Ⅱ的反应类型为加聚反应。


科目:高中化学 来源: 题型:
【题目】S转化为H2SO4有下列两种途径,部分反应条件和产物已省略。
途径①:S![]() H2SO4
H2SO4
途径②:S![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
下列有关说法不正确的是 ( )
A. 途径①的反应体现了浓硝酸的强氧化性和酸性
B. 途径②中有两步氧化还原反应
C. 由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol电子
D. 理论上,途径②相比途径①对环境的污染小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 1mol甲基中含有电子数为10NA
B. 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA
C. 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA
D. 50mL12mol·L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从柑橘中可提炼得1,8萜二烯(![]() ).下列有关它的说法正确的是( )
).下列有关它的说法正确的是( )
A. 分子式为C10H14
B. 属于烃,难溶于水,可用某些有机溶剂提取1,8萜二烯
C. 与酸性高锰酸钾溶液、氧气、溴水等均可发生氧化反应
D. 它的一种同分异构体的结构中可能含有苯环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.将等物质的量的A和B,混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),5min 后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(Lmin)。
xC(g)+2D(g),5min 后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(Lmin)。
(1)B的反应速率v(B)=_____________,X=_____。
(2)A在5min末的浓度是________________。
(3)此时容器内的压强与开始时之比为_________。
Ⅱ.(4)二氯化二硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式____________;
b.指出它分子内的键型_________。
(5)硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是___________。
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是________(填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15L 6.0mol·L-1的盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。请填空:
(1)①中引发铝热反应的实验操作是____________,产物中的单质B是________。
(2)②中所发生的各反应的化学方程式是________________。
(3)③中所发生的各反应的离子方程式是________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为______,c(Fe2+)为_____。(保留小数点后两位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用可以制备金属镁,其流程如下图所示:

(1)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。_______________________
(2)实验室将粗盐制成精盐的过程中,溶解、过滤、蒸发三个步骤的操作都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
①溶解:_____________________________。
②过滤:_____________________________。
③蒸发:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存而且为无色透明的溶液是( )
A.NH4+、Al3+、SO42﹣、NO3﹣
B.K+、Na+、NO3﹣、CO32﹣
C.K+、MnO4﹣、NH4+、NO3﹣
D.H+ , K+ , OH﹣ , NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com