
【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍 | 试通过计算填空: (1)A的相对分子质量为____ |
(2)将9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | (2)A的分子式为_____ |
(3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) | (3)用结构简式表示A中含有的官能团:___________________________ |
(4)A的核磁共振氢谱如图:
| (4)A中含有____种氢原子 |
(5)综上所述,A的结构简式为______,请写出A与NaHCO3反应的化学方程式______ | |
【答案】 90 C3H6O3 —COOH、—OH 4 ![]()
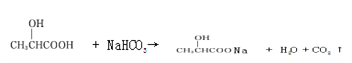
【解析】(1)A蒸气密度是相同条件下H2的45 倍,则A的相对分子质量为45×2=90;(2) 9.0gA的物质的量是0.1mol,在足量纯O2中充分燃烧,并使一其产物依次缓缓通过浓硫酸吸收水分,增重5.4g,则n(H2O)=5.4g÷18g/mol=0.3mol;通过碱石灰吸收CO2,增重13.2g,则n(CO2)=13.2g÷44g/mol=0.3mol,其中含有O元素的物质的量是n(O)=(9.0g-0.3mol×2×1g/mol-0.3mol×12g/mol)÷16g/mol=0.3mol,所以根据原子守恒可知A分子式为C3H6O3;(3)另取A9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),n(CO2)=2.24L÷22.4L/mol=0.1mol,说明一个分子中含有一个羧基;若与足量金属钠反应则生成2.24LH2(标准状况),n(H2)=2.24L÷22.4L/mol=0.1mol。由于钠与羧基和羟基都可以发生置换反应产生氢气,所以说明分子中还含有一个羟基,因此A中所含官能团的名称羧基、羟基;(4)根据A 的核磁共振氢谱图可知:在该物质分子中含有4种不同的氢原子,个数比是1:1:1:3;(5)根据上述分析可知A结构简式是![]() 。A与NaHCO3反应的化学方程式为CH3CHOHCOOH+NaHCO3→CH3CHOHCOONa+CO2↑+H2O。
。A与NaHCO3反应的化学方程式为CH3CHOHCOOH+NaHCO3→CH3CHOHCOONa+CO2↑+H2O。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是( )
A. 浓硫酸和浓盐酸长期暴露在空气中浓度降低
B. 氯水和活性炭使红墨水褪色
C. 铁片和铝片置于冷的浓硫酸中均无明显现象
D. 二氧化硫和过氧化钠使品红褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿主要成分是A12O3,含杂质SiO2、Fe2O3。 工业上从铝土矿中提取铝可采取如下工艺流程:
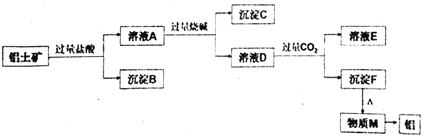
请回答下列问题:
(1)写出铝土矿溶解于过量盐酸的离子方程式___________________________________。
(2)写出溶液A中加过量烧碱的离子方程式___________________________________。
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于反应:2NO(g)+O2(g)![]() 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图)。
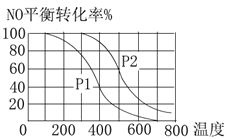
①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________(填“增大”或“减小”)。
(2)在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),已知随温度升高,此混合气体的颜色变深。
2NO2(g),已知随温度升高,此混合气体的颜色变深。
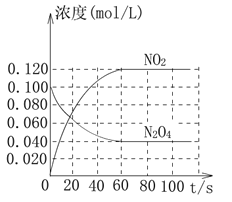
回答下列问题:
①反应的ΔH_________________________(填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为____________mol·L-1·s-1;反应的平衡常数K1为____________________。
②100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。列式计算温度T时反应的平衡常数K2=_________________。
③温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________________(填“正反应”或“逆反应”)方向移动,判断理由是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,以达到保鲜的目的
B. 天然气的主要成分是丙烷
C. 糖尿病患者不可以用新制备的氢氧化铜检验
D. 煤的干馏是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日本地震引起的核泄漏中放射性物质主要是Cs和131I,其中有关127I与131I的说法正确的是( )
A. 127I与131I互为同位素 B. 127I与131I互为同素异形体
C. 127I与131I是同分异构体 D. I与Cl均属ⅦA族,I比Cl活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、G、H、I均为气体,G可使湿润红色石蕊试纸变蓝,J为常见的液态物质,A、B、C、I、M为单质,且M为常见金属,G和H相遇时产生白烟,它们存在如下的转化关系(图中部分反应物或产物已省略),请回答有关问题: 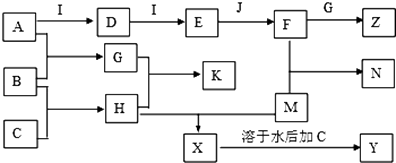
(1)请写出:A物质的化学式: , K物质的名称: , 例举F物质的一种用途;
(2)①写出实验室用K制取G的化学方程式; ②实验室检验气体G是否收集满的方法:;
③G与H相遇可生成白烟K,请写出该反应的化学方程式 .
(3)①F的浓溶液与木炭反应的化学方程式为; ②工业F的浓溶液呈黄色,试用化学方程式解释原因:;
若要消除黄色可向其中通入一定量的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是

A. b点时,CO的转化率为20%
B. 容器内的压强保持恒定,表明反应达到平衡状态
C. b点和d点的化学平衡常数:Kb>Kd
D. 0到0.5min反应速率v(CO)=0.3mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com