
【题目】将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是
A. c(NH4+)>c(Cl–)>c(H+)>c(OH–) B. c(NH4+)>c(Cl–)>c(OH–)>c(H+)
C. c(Cl–)>c(NH4+)>c(H+)>c(OH–) D. c(Cl–)>c(NH4+)>c(OH–)>c(H+)
科目:高中化学 来源: 题型:
【题目】CO2回收资源化利用是环保领域研宄的热点课题,
(1)在FeO催化下,以CO2为原料制取炭黑(C)的太阳能工艺如图1所示。
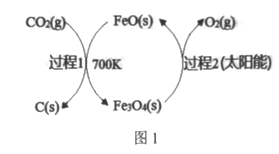
己知:①过程1生成lmolC(s)的反应热为△H1。
②过程2反应:Fe3O4(s)![]() 3FeO(s)+l/2O2(g) △H2。
3FeO(s)+l/2O2(g) △H2。
上述以CO2为原料制取炭黑总反应的热化学方程式为____________,若该反应的△S<0,请判断
该反应是否为自发反应并说明理由___________________。
(2)以CO2为原料可以催化加氢合成低碳烯烃,利用CO2合成乙烯的反应方程式为:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g) △H3。在常压下,以 FeCoMnK/BeO 作催化剂,按n(CO2): n(H2)=l:3(总物质的量为4amol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图2所示。
C2H4(g)+4H2O(g) △H3。在常压下,以 FeCoMnK/BeO 作催化剂,按n(CO2): n(H2)=l:3(总物质的量为4amol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图2所示。
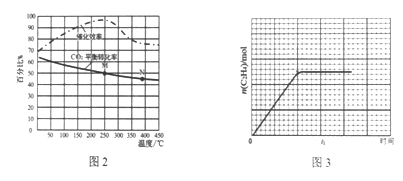
①下列说法不正确的是______________。
A. △H3<0;平衡常数:KM >KN
B.增加原催化剂的表面积,对平衡转化率无影响
C.生成乙烯的速率:v(M)有可能小于v(N)
D.若投料比改为n(CO2):n(H2)=1:2,可以提高CO2的平衡转化率
E.若投料比不变,温度越低,反应一定时间后CO2的转化率越高
②250℃下,上述反应达平衡时容器体积为VL,则此温度下该反应的平衡常数为___________(用含a、V的代数式表示)。
③某温度下,n(C2H4)随时间(t)的变化趋势曲线如图3所示。其它条件相同时,若容器的体积为其一半,画出0~t1时刻n(C2H4)随时间(t)的变化趋势曲线。______
(3)以稀硫酸为电解质溶液,利用太阳能可将CO2电解转化为低碳烯烃,则电解生成丙烯时,阴极的电极反应为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完成下列表格
主要物质 | 杂质 | 除杂试剂 | 操作名称 |
CO2气体 | HCl气体 | _______ | _______ |
FeCl2溶液 | CuCl2 | _______ | _______ |
水 | 花生油 | _______ |
(2)用双线桥法表述(只标注电子转移情况):MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O___________。
MnCl2+Cl2↑+2H2O___________。
用单线桥法表述电子转移情况:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O___________。
(3)用所给量的符号和必要的数据,按要求列出相关计算式:
①摩尔质量为M,气体摩尔体积为Vm,则气体体积V与气体质量m的关系___________。
②物质的量浓度为c,溶质摩尔质量为M,则溶液体积V与所含溶质质量m的关系____。
③溶质摩尔质量为M,溶液密度为dg/ml,则物质的量浓度c与溶质质量分数a%的关系c=__。
④摩尔质量为M,气体摩尔体积为Vm,则气体的密度=______________。
⑤某条件下气体摩尔体积为Vm,将V升某气体(摩尔质量为M)溶于1升水,得到密度为dg/mL的溶液,则该溶液的物质的量浓度c=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为( )
A. A﹥B﹥E﹥D B. A﹥B﹥D﹥E
C. D﹥A﹥B﹥E D. D﹥E﹥A﹥B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面对氯气的叙述正确的是
A.氯气可使湿润的红布条褪色,所以氯气具有漂白性
B.氯气没有漂白性,但通入品红溶液中,品红褪色
C.过量的铜在氯气中燃烧可生成氯化亚铜
D.闻其气味时要小心的将集气瓶放在鼻孔下直接闻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用下列图Ⅰ装置进行铜跟浓硫酸反应等一系列实验。
请回答:
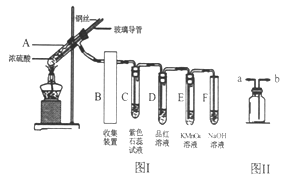
(1)图I装置中的收集装置B应连接图Ⅱ中的__________(填“a”或“b”)进口。
(2)用此装置制SO2与将铜片直接加入试管A加热反应相比,其优点主要是______________。
(3)下列叙述中,描述正确的是______________。
A.A试管中发生了Cu与浓硫酸的反应,其中浓硫酸只体现了强氧化性
B.熄灭酒精灯后,因为A试管中的玻璃导管存在,整套装置不易发生倒吸
C.C试管中的紫色石蕊试液会变红,是因为二氧化硫溶于水后生成了 H2SO3
D.D、E试管中品红和高锰酸钾溶液都会褪色,其褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 电解稀H2SO4、Cu(NO3)2、NaCl的混合液,最初一段时间阴极和阳极上分别析出的物质分别是( )
A.H2和Cl2 B.Cu和Cl2 C.H2和O2 D.Cu和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 X、Y、Z是三种常见元素的单质,甲乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是
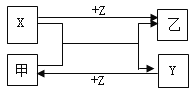
A. X、Y、Z都是非金属单质
B. X、Y、Z中至少有一种是金属单质
C. 如果X、Y都为非金属单质,则Z必为金属单质
D. 如果X、Y都为金属单质,则Z必为非金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是周期表的一部分,其中X、Y、Z、W为短周期主族元素,下列说法正确的是
X | Y | ||
Z | W |
A. W的最高价氧化物对应的水化物一定是强酸 B. Z的单质一定能溶于稀硫酸中
C. 四种元素的最高正化合价均等于其族序数 D. 四种原子中,Z的原子半径最小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com