
在实验室进行物质制备,下列从原料及有关试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合 理的是
理的是
A.C CO
CO CO2
CO2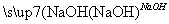 Na2CO3
Na2CO3
B.Cu Cu(NO3)2溶液
Cu(NO3)2溶液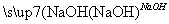 Cu(OH)2
Cu(OH)2
C.CaO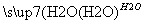 Ca(OH)2溶液
Ca(OH)2溶液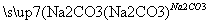 NaOH溶液
NaOH溶液
D.Fe Fe2O3
Fe2O3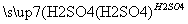 Fe2(SO4)3溶液
Fe2(SO4)3溶液
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3比较中,下列说法不正确的是
A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解
B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多
C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深
D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用下列装置进行乙醇催化氧化的实验。
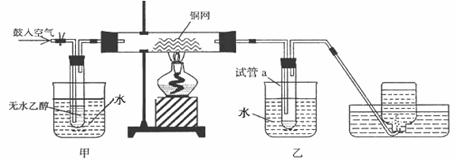
(1)、实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,
说明该乙醇催化反应是_____ 反应。
(2)、甲和乙两个水浴作用不相同。
甲的作用是____________; 乙的作用是_______________。
(3)、反应进行一段时间后,干燥试管a中能收集到不同的物质,
它们是 __。
集气瓶中收集到的气体的主要成分是____________ 。
(4)、试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________________ 。
要除去该物质,可在混合液中加入_____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过___________________(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为探究SO2与Ba2+只有在碱性条件下才能形成BaSO3沉淀,设计了如下方案,你认为可行的是
A.将SO2通入Ba(OH)2溶液中观察有白色沉淀生成
B.将SO2通入Ba(NO3)2溶液中观察有白色沉淀生成
C.将SO2分别通入BaCl2溶液、BaCl2与HCl的混合溶液、Ba(OH)2溶液中,观察到只有Ba(OH)2中有白色沉淀生成
D.将SO2通入BaCl2与NH3的混合溶液中有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.一般认为沉淀离子浓度小于10-5 mol/L时,则认为已经沉淀完全
B.反应AgCl+NaBr===AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3
Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡
Al3++3OH-表示水解平衡
D.只有反应速率很高的化学反应才能应用于工业生产
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O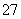 和CrO
和CrO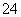 ,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
CrO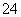
 Cr2O
Cr2O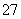
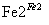 Cr3+
Cr3+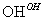 Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:
2CrO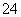 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O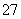 (橙色)+H2O
(橙色)+H2O
(1)若平衡体系的 pH = 2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是________。
a.Cr2O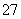 和CrO
和CrO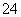 的浓度相同
的浓度相同
b.2v(Cr2O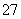 )=v(CrO
)=v(CrO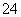 )
)
c.溶液的颜色不变
(3)第②步中,还原 1 mol Cr2O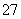 离子,需要________mol的FeSO4·7H2O。
离子,需要________mol的FeSO4·7H2O。
(4)第 ③步生成的Cr(OH)3 在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)  Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3 的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使 c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使 c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
方法2:电解法
该法用 Fe 做电极电解含Cr2O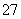 的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3 沉淀。
的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3 沉淀。
(5)用Fe做电极的原因为_____________________ _______________________。
_______________________。
(6)在阴极附近溶液 pH 升高的原因是(用电极反应解释)________,溶液中同时生成的沉淀还有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com