
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| ƽ��� | a | b | c | d |
| ƽ��� | m | n | x | y |
���� ��1��H2������������¶ȵ����߶����ӣ���˵�������¶�ƽ���淴Ӧ������У�������Ӧ�Ƿ��ȷ�Ӧ�������¶������淴Ӧ���ʾ�����ƽ���淴Ӧ������У�ƽ�ⳣ����С����Ӧ���ת���ʼ�С��
��2����ͬ�¶�ʱƽ�ⳣ�����䣬��K=$\frac{c{d}^{2}}{a{b}^{4}}$=$\frac{x{y}^{2}}{m{n}^{4}}$��
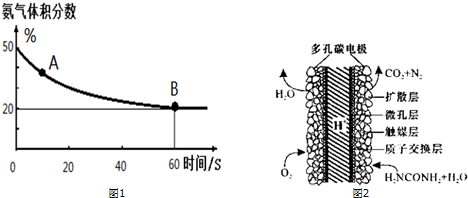
��3������ƽ���֪�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ�е�pH�������䣻�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䣻
��4��9 mol CO2���ܷ���ں�KO2��Ӧ������9 mol O2����n��CO2����n��O2��=1��1��������������ʽ��ӵõ�8KO2+6CO2+2H2O��2K2CO3+4KHCO3+6O2�����ݷ���ʽ��������ˮ������
��� �⣺��1��H2������������¶ȵ����߶����ӣ���˵�������¶�ƽ���淴Ӧ������У�������Ӧ�Ƿ��ȷ�Ӧ�������¶������淴Ӧ���ʾ�����ƽ���淴Ӧ������У�ƽ�ⳣ����С����Ӧ���ת���ʼ�С��
�ʴ�Ϊ����������С����С��
��2����ͬ�¶�ʱƽ�ⳣ�����䣬��a��b��c��d��m��n��x��y֮��Ĺ�ϵʽΪ��K=$\frac{c{d}^{2}}{a{b}^{4}}$=$\frac{x{y}^{2}}{m{n}^{4}}$��
�ʴ�Ϊ��$\frac{c{d}^{2}}{a{b}^{4}}$=$\frac{x{y}^{2}}{m{n}^{4}}$��
��3������ƽ���֪�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ�е�pH�������䣻�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䣬
�ʴ�Ϊ���������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ�е�pH�������䣻�������������ʽ���ѪҺ�У�ƽ�������ƶ���ʹH+Ũ�ȱ仯��С��ѪҺ��pH�������䣻
��4���������ַ������
����һ�������⣬9 mol CO2���ܷ���ں�KO2��Ӧ������9 mol O2����n��CO2����n��O2��=1��1��ͨ���۲������������ʽ��֪��������������ʽ���ʱ���÷�����ĿҪ��8KO2+6CO2+2H2O��2K2CO3+4KHCO3+6O2
������n��H2O��=$\frac{1}{3}$n��CO2��=$\frac{1}{3}$��9mol=3mol������Ӧǰ�ܷ����H2O�����ʵ���Ϊ3mol��
���������跴Ӧǰ�ܷ����H2O�����ʵ���Ϊn
4KO2+4CO2+2H2O��4KHCO3+3O2
2n n 1.5n
4KO2+2CO2��2K2CO3+3O2
9-2n 1.5��9-2n��
����������������9mol��������1.5n+1.5��9-2n��=9mol�����n=3mol������Ӧǰ�ܷ����H2O�����ʵ���Ϊ3mol��
�ʴ�Ϊ��3mol��
���� ���⿼���Ϊ�ۺϣ��漰��ѧƽ�ⳣ��������Ũ�ȴ�С�Ƚ��Լ�������ʵĵ����֪ʶ��Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ��������������Ŀ��飬ע�����ƽ�ⳣ�������壬��Ŀ�Ѷ��еȣ�


 Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
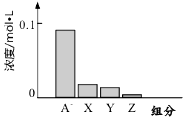 �����£�0.2mol/L��һԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�������Һ�ж�������ּ�Ũ����ͼ��ʾ������˵����ȷ���ǣ�������
�����£�0.2mol/L��һԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�������Һ�ж�������ּ�Ũ����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | HAΪǿ�� | B�� | �û��ҺpH=7 | ||
| C�� | ͼ��X��ʾHA��Y��ʾOH-��Z��ʾH+ | D�� | �û����Һ�У�c��A-��+c��Y��=c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ��������Ũ�� ��10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Ⱦ��ָ����ϩ��������ϩ���������� | |
| B�� | ��֬�����������ʣ���һ����Ȼ�л��߷��ӻ����� | |
| C�� | ��ȡ����������������ֹʹ�������ã�����������к��������������ڶ�Ʒ | |
| D�� | �������벻�㣬������Ѫ�ǣ���������࣬�������������Ӳ�������IJ��ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �γɺϽ�����۵�Ҫ��� | B�� | �Ͻ��ǻ���� | ||
| C�� | �Ͻ���й̶����۵� | D�� | ����ǽ����ȣ����Ⱥ����γɺϽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com